题目内容
【题目】(6分)氧化钙俗名生石灰,某同学针对氧化钙设计了如下实验方案:
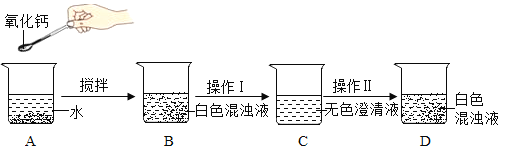
(1)A中发生反应的化学方程式为___________。分离B中难溶物的操作I叫_________。
(2)如果要用实验证明C中不是水而是一种溶液,可以选择下列______(填序号)进行试验。
①稀盐酸 ②酚酞溶液 ③二氧化碳 ④氯化钠溶液
(3)操作II是加入某种物质使无色澄清液出现白色固体,如果加入的是饱和碳酸钠溶液,白色固体的化学式是___________;如果加入的是固体氢氧化钠(全部溶解),白色固体的化学式是___________。
【答案】(1)CaO + H2O == Ca(OH)2 过滤 (2)②③ (3)CaCO3 Ca(OH)2
【解析】
试题分析:(1)A中是将氧化钙加入到水中,发生反应的化学方程式为:CaO + H2O == Ca(OH)2 ;分离B中难溶物的操作I叫过滤
(2)如果要用实验证明C中不是水而是一种溶液,实际就是氢氧化钙溶液,根据氢氧化钙的化学性质:能使无色酚酞溶液变红;二氧化碳能使氢氧化钙溶液变浑浊,稀盐酸虽然能与氢氧化钙溶液反应,但是没有明显现象,氯化钠溶液不能与氢氧化钙溶液反应,故选②③
(3)操作II是加入某种物质使无色澄清液出现白色固体,如果加入的是饱和碳酸钠溶液,发生的反应:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH,所以白色固体的化学式是CaCO3;如果加入的是固体氢氧化钠(全部溶解),由于固体氢氧化钠溶于水放热使温度升高,而氢氧化钙的溶解度随温度的升高而降低,温度升高溶质氢氧化钙结晶析出,所以白色固体的化学式是:Ca(OH)2

练习册系列答案
相关题目