题目内容
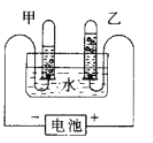
【题目】为验证氢氧化钙的部分化学性质,设计如图实验进行探究。
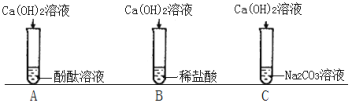
(1)实验A 证明氢氧化钙具有的化学性质是_____。
(2)三组实验中不能判断反应能发生的是_____ 。在此实验的基础上,利用现有试剂验证该反应一定发生。写出操作步骤和预期现象_________。
(3)完成上图实验后,将三支试管中所有物质倒入烧杯中,观察到溶液呈无色且浑浊,写出溶液中溶质成分的可能组成(酚酞除外)_________。
【答案】显碱性 B 向 B 试管中滴入酚酞溶液,酚酞不变色;若酚酞变红,再向其中逐滴滴入稀盐酸至溶液恰好由红色变为无色 NaCl;NaCl、CaCl2
【解析】
(1)将氢氧化钙溶液滴加到酚酞溶液中,可以观察到酚酞溶液变红,说明氢氧化钙溶液呈碱性,故填显碱性。
(2)实验A中观察到溶液变红,实验B中氢氧化钙与盐酸反应生成氯化钙和水,无明显变化,无法判断是否发生反应,实验C中氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,有白色沉淀生成,所以三组实验中不能判断反应能发生的是B,故填B;
为判断B中是否发生反应,可向反应后的液体中滴加滴入酚酞溶液,若酚酞不变色,说明氢氧化钙不存在,表明氢氧化钙与盐酸发生了反应,若酚酞变红,再向其中逐滴滴入稀盐酸至溶液恰好由红色变为无色,说明氢氧化钙能够与盐酸反应,故填向 B 试管中滴入酚酞溶液,酚酞不变色;若酚酞变红,再向其中逐滴滴入稀盐酸至溶液恰好由红色变为无色。
(3)实验后,将三支试管中所有物质倒入烧杯中,观察到溶液呈无色,说明溶液中氢氧化钙、碳酸钠均不存在;碳酸钙与盐酸反应生成可溶的氯化钙、水和二氧化碳,溶液浑浊,说明盐酸没有剩余;溶液变浑浊是因为B中反应生成的氯化钙与C中的碳酸钠反应生成碳酸钙沉淀和氯化钠,所以溶液中的溶质一定含有氯化钠,还可能有氯化钙剩余,则溶液中溶质的存在情况是氯化钠或者是氯化钙与氯化钠,故填NaCl;NaCl、CaCl2。

 小学教材全测系列答案
小学教材全测系列答案【题目】铜粉中混有少量的铁粉,为了除去铁粉,某校兴趣小组同学,取该铜粉20g于烧杯中,然后等量分5次加入未知质量分数的某强酸(W)溶液,充分反应后所得数据如下表,请根据相关知识和图表信息回答下列问题。
项目 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入W溶液的质量/g | 5 | 5 | 5 | 5 | 5 |
每次产生气体的质量/g | 0.01 | 0.01 | 0.01 | 0.005 | 0 |
(1)写出你所选择酸(W)的化学式 。
(2)铜粉中混有铁粉的质量是 。
(3)计算你选择酸(W)的质量分数(写出计算过程)。