题目内容
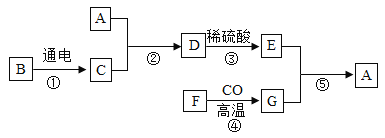
【题目】氯碱工业以粗盐(主要成分是NaCl, 含少量泥沙、CaCl2、 MgCl2)为原料,生产氯气和氢氧化钠,模拟流程如下:
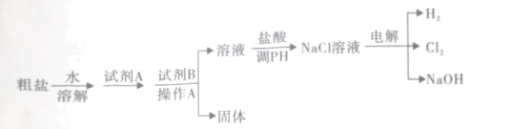
(1)试剂A与试剂B的组合为____________(填序号)
①KOH
②NaOH
③K2CO3
④Na2CO3
(2)操作A中用到的玻璃仪器有哪些___________?
(3)写出电解NaCl溶液的化学方程式___________。
【答案】②④ 烧杯、漏斗、玻璃棒 
【解析】
(1)含有氯化钙、氯化镁等物质,可以利用碳酸根与钙离子生成碳酸钙沉淀,镁离子与氢氧根离子、碳酸根离子反应生成碳酸镁和氢氧化镁沉淀,选择含有碳酸根和氢氧根离子的试剂,因为制备氢氧化钠,所以加入阳离子为钠离子即可,避免引入其他杂质,所以选择氢氧化钠和碳酸钠。故答案为:②④。.
(2)操作A实现了固液分离,采用操作为过滤,过滤利用玻璃仪器为烧杯盛取滤液,玻璃棒引流滤液,漏斗过滤滤液。故答案为:烧杯、漏斗、玻璃棒。
(3)反应物有氯化钠,生成物有氢氧化钠、氯气和氢气,反应物缺少氢元素和氧元素, 因此反应物还需要水,所以氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,据此书写化学方程式。故答案为: 。
。

【题目】有一包固体物质,可能含有硫酸钠、碳酸钙、氯化钾、碳酸钠、硫酸铜和氢氧化钠中的一种或几种。为探究其组成,进行如下实验。
(1)取少量固体按以下流程实验

根据步骤①可知固体中一定不含有_______________(填化学式)。
(2)向白色沉淀B中滴加过量稀盐酸,发现仍有部分固体剩余;则固体物质中的成分中一定有的是________(填化学式)。
(3)为进一步确定固体中可能含有的物质,兴趣小组进行如下探究:
[猜想与假设]
猜想一:氯化钾
猜想二:氢氧化钠
猜想三:_________________
实验操作 | 实验现象 | 结论与评价 |
1. 取少量溶液C于试管,滴加无色酚酞试液 | __________ | 猜想一不成立 |
2.另取少量溶液C于试管,滴加过量稀硝酸后,再滴加___________溶液 | __________ | 猜想三成立 |
[反思交流]工业流程步骤②中不能将Ba(NO3)2溶液换成Ba(OH)2溶液的原因是:__________________。