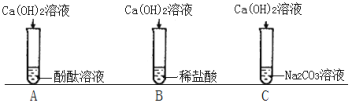
题目内容
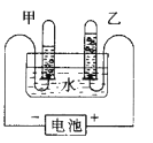
【题目】向98g水中加入20g溶质质量分数为9.8%的稀硫酸,进行电解水的实验。实验结束后,甲试管里收集到0.02 g气体。请完成下列分析及计算:
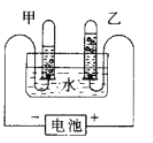
(1)若电解前测得溶液的pH为a,一段时间后测得溶液的pH为b,则a (选填“大于”“等于”或“小于”)b。
(2)实验结束后所得溶液中溶质的质量分数(结果精确到0. 1%)。
【答案】(1)大于(2)1. 7%
【解析】
解:(1)电解过程中,水的质量不断减少,稀硫酸的浓度不断增大,溶液的酸性增强,pH变小,故电解前测得溶液的pH为a,一段时间后测得溶液的pH为b,则a大于b。
(2)设生成0.02 g氢气需分解水的质量为![]()
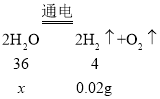
![]()
解得![]() =0.18g
=0.18g
实验结束后所得溶液中溶质的质量分数为![]()
答:实验结束后所得溶液中溶质的质量分数为1. 7%。

 习题精选系列答案
习题精选系列答案【题目】有一包固体物质,可能含有硫酸钠、碳酸钙、氯化钾、碳酸钠、硫酸铜和氢氧化钠中的一种或几种。为探究其组成,进行如下实验。
(1)取少量固体按以下流程实验

根据步骤①可知固体中一定不含有_______________(填化学式)。
(2)向白色沉淀B中滴加过量稀盐酸,发现仍有部分固体剩余;则固体物质中的成分中一定有的是________(填化学式)。
(3)为进一步确定固体中可能含有的物质,兴趣小组进行如下探究:
[猜想与假设]
猜想一:氯化钾
猜想二:氢氧化钠
猜想三:_________________
实验操作 | 实验现象 | 结论与评价 |
1. 取少量溶液C于试管,滴加无色酚酞试液 | __________ | 猜想一不成立 |
2.另取少量溶液C于试管,滴加过量稀硝酸后,再滴加___________溶液 | __________ | 猜想三成立 |
[反思交流]工业流程步骤②中不能将Ba(NO3)2溶液换成Ba(OH)2溶液的原因是:__________________。