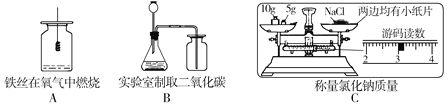
��Ŀ����
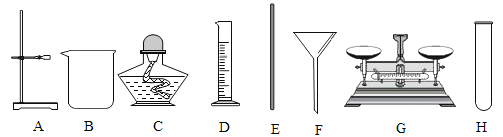
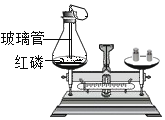
����Ŀ����������ʵ��װ�ã���ͼ1��ʾ���ش����⣺
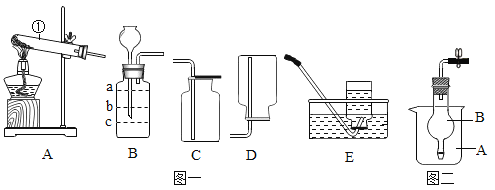
��1�������ٵ�������____________�����ڼ��ȵ�������_____________________��
��2������Bװ�������壬����Һ���λ����_________������װ���е���ĸ����
��3��ʵ���������������������5%��˫��ˮ��Һ��Ӧ������Ҳ�ܿ��ٲ������壬�ҷ�Ӧ��������˳���������ظ�ʹ�á���д���÷�Ӧ�Ļ�ѧ����ʽ________________________�������ڸ÷�Ӧ�е�������____________��
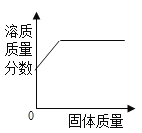
��4��������ȡ0.05mol��������Ҫ������������ʵ���Ϊ__________��Ҫ��д��������̣�������������������Ϊ5%�Ĺ���������Һ��ȡ������������Ҫ��Һ������Ϊ_________g.
��5����ʵ����������غͶ������̵Ļ������ȡ���ռ���������ѡ��ķ���װ��Ϊ_________������ĸ������Ӧ�Ļ�ѧ����ʽΪ________________________��
���𰸡��Թ� �ƾ��� b 2H2O2 2H2O+O2�� ������ 0.1mol 68g A 2KClO3
2H2O+O2�� ������ 0.1mol 68g A 2KClO3![]() 2KCl+3O2����
2KCl+3O2����
��������
��1��ͨ������������ָ���������ÿ�֪�������Թܣ����ڼ��ȵ������Ǿƾ��ƣ�
��2������Bװ�������壬����©�����¶�Ӧ����Һ�����£��Է�����ӳ���©���ݳ����ʼ���Һ���λ����b����
��3����������������Ĵ������·ֽ�����ˮ����������ѧ����ʽΪ��2H2O2 2H2O+O2���������Ǹ÷�Ӧ�Ĵ�����������á�
2H2O+O2���������Ǹ÷�Ӧ�Ĵ�����������á�
��4���⣺���������������ʵ���Ϊxmol
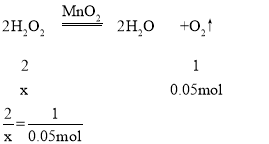
x=0.1mol ����Ϊ3.4g
���Զ�Ӧ�Ĺ���������Һ������Ϊ3.4g��5%�T68g
��5������غͶ������̶��ǹ��壬��Ӧ�����Ǽ��ȣ�����װ��ѡ��A����ѧ����ʽΪ��2KClO3![]() 2KCl+3O2����
2KCl+3O2����
�ʴ�Ϊ��
��1���Թܣ��ƾ��ƣ�
��2��b��
��3��2H2O2 2H2O+O2���������ã�
2H2O+O2���������ã�
��4��0.1mol��68g��
��5��A��2KClO3![]() 2KCl+3O2����
2KCl+3O2����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ���ÿ�ѧ������ʶ�������ʡ��������̽������գ����տ�ѧ��ʶ�Ĺ��̣���ѧ������Ҫ�̺��������Σ�һ�Ǹ�����ʶ�Σ���Ҫ��Ϊ�˻��֤�ݣ���۲졢Ԥ�⡢ʵ��ȣ�����������ʶ������˼ά���Σ���Ҫ��Ϊ���γɿ�ѧ��ʶ�����ѧ����ѧ��˵����Ƚ���Աȡ�����������ȡ���ǰһ�ε�ѧϰ�У�����ͨ��ʵ�顢�۲���ֶ���֤�˺ܶѧ��Ӧ�ķ����������������ɡ�����Ƚϡ��Ա����ȿ�ѧ��һ�㷽����ʶ�˼��ֵ��͵��ᡢ��Ρ������������Ϸ�����ʶ����ͭ��
��1���ù���/����ķ�����ʶ����ͭ�Ļ�ѧ������֪���з�Ӧ��
H2SO4+BaCl2�TBaSO4��+2HClNa2SO4+BaCl2=BaSO4��+2NaCl
MgSO4+BaCl2�TBaSO4��+MgCl2K2SO4+BaCl2=BaSO4��+2KCl
�ٴ��۷������鷴Ӧ�ܹ�������ԭ����_____��
���ɢ��еõ��Ĺ��ɿ�������������ͭ��ҺҲ�ܸ��Ȼ�����Һ��Ӧ�������õ���_____�ķ�����
��2����ʵ��ķ�����ʶ����ͭ�Ļ�ѧ����������֤��1������������ͭ��ҺҲ�ܸ��Ȼ�����Һ��Ӧ�������ۣ������ʵ���ǣ�
ʵ����� | ʵ������ | ���� |
ȡ��������ͭ��Һ��A�Թ��У�Ȼ���ٵμ��Ȼ�����Һ | _____ | ���ۣ�����ͭ��Һ�ܸ��Ȼ�����Һ��Ӧ |
����ʵ��ķ�����ʶ����ͭ����������
ʵ����� | ʵ������ | ���� |
ȡ��������ͭ��Һ��B�Թ��У�Ȼ���ٵμ�2��3����ɫʯ����Һ���� | ʯ����Һ��� | ���ۣ�����ͭ��Һ��_____ |
ȡ��������ͭ��Һ��C�Թ��У�Ȼ���ٵμ�����������Һ | _____ | ���ۣ�_____ |
��3������Ҫ��ѧ��ʵ�鷽����������ѧת���������������������û�ѧ�仯���������������Ҫ�����ʣ�����شٽ����������ķ�չ�����ǵ����Ⱥ���������˶�����ͭ���ա�
������ͭ������ȸʯ����Ҫ�ɷ���Cu2(OH)2CO3����ľ̿һ����ȿ��Եõ���ɫ�Ľ���ͭ����д��������Ӧ�Ļ�ѧ����ʽ����_____����_____����������ʾ:��ȸʯ�����ֽ⣬�õ�����ͭ��������̼��ˮ���ڼ��ȵ�������ľ̿������ͭ��Ӧ�õ�ͭ�Ͷ�����̼����
��ʪ����ͭ������Ȼͭ�Ļ��������ʪ����ͭ����������������ͭ��Ӧ���������û���ͭ�������������Ϊͭ������������ָ������ͭ�Σ���ͭ��������������ͭ���ɡ���д��������Ӧ�Ļ�ѧ����ʽ����_____����_____����������ʾ����������������ͭ��Ӧ�õ�������ͭ�Σ�ͭ������������ͭ���ɡ���
����Ŀ�������ϣ���ʦ��ͬѧ��̽���˶�����̼�����ʡ���ش����⡣
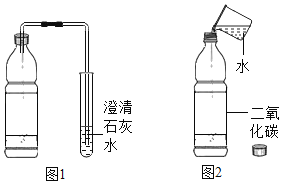
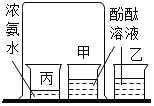
��ѧϰ�龰������ˮƿ��ʱ��������ð����ͬѧ�ǽ�����ͨ�����ʯ��ˮ�У�ʯ��ˮ����ǣ���ͼ����������Ӧ�Ļ�ѧ����ʽ��_______________��ʵ�����ʦҪ��ͬѧ�ǽ��Թ��еĻ������ٴα�ó��壬����Ϊ�ɲ��õķ�����____________________��
���������һ����ˮ��Ϊʲô�����������̼�����أ�
���������룩��ˮ�����ж�����̼��������̼������ˮ��
������ʵ�飩��һ���ռ���������̼������ʵؽ���������ƿ�м���![]() �����ˮ������š��ƿ�ǣ����۲쵽��������_________________���ó�������̼������ˮ�Ľ��ۡ�
�����ˮ������š��ƿ�ǣ����۲쵽��������_________________���ó�������̼������ˮ�Ľ��ۡ�
����������������������ˮ�Ĺ������Ƿ���ˮ�����˻�ѧ��Ӧ��
���������룩������̼����ˮ������ѧ��Ӧ�������������ʡ�
��ʵ�鷽����ȡ��������ɫʯ����ҺȾ����ɫ�ĸ���ֽ�����������ʵ�顣
ʵ����� | ʵ������ѧ����ʽ | ʵ����� |
����һ������һ��ֽ������ϡ���� | ������ɫֽ����� | ���ۣ�������̼����ˮ������ѧ��Ӧ����ѧ����ʽ______________�� |
����������ڶ���ֽ��ֱ�ӷ���ʢ�M����̼�ļ���ƿ�С� | ������ɫֽ��û�б�� | |
����������������ֽ���� ��ˮ���ٷ���ʢ��������̼�ļ���ƿ�� | ���� _________ | |
�����ģ�������������ƿ �е�ֽ��ȡ�����ô������� | ���� _________ | ���ۣ� ________ |
��ʵ���ܽᣩ��ˮΪ�������ٺ��������������ʣ�______�����û�ѧʽ��ʾ��
����Ŀ��ʵ�����зֱ��ø�����ء��������⡢�������ȡ�Ƚϴ��������������㰴��Ҫ��ش����⣺
��1�����ͼ1���ṩװ��������б���
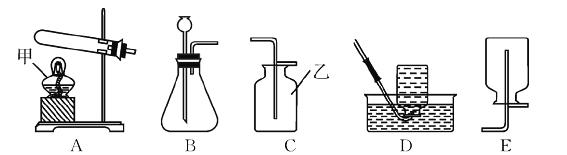
��Ӧ����д���� | ��Ӧ�����ֱ���ʽ | ������ȡװ�����(�����) |
��������(��������) | ������������ | ____ |
������� | __________________ | ____ |
�����(��������) | _______________________ |
��2������ͼ1�ش����⣺
��д���ס�����ָ�������ƣ���_____����_______��
���ù���������������װ�����������ַ�����װ����Ⱦ��е��ŵ���______��______ (д������)��
������ͼ2װ���ռ�һƿ����������Ӧ��______ (�a����b��)�˽��뼯��ƿ��
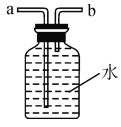
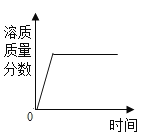
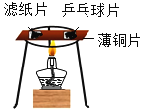
��3��С��Ϊ���о��������ſ���������ˮ���ռ�������Ũ���Ƿ��в��죬��������ʵ�飺���ȸ�����ع��壬�ֱ������ַ������ռ���ƿ��������ʹ�ô������ⶨ�ռ���������Ũ�ȣ����ݼ�����
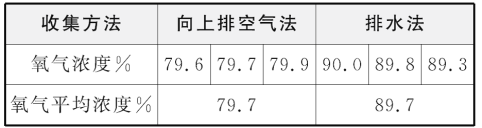
��С���������ſ������ռ�����ʱ������ʹ�����ڼ���ƿƿ�ڵĴ�����ľ����ȼΪ���������ı�������ˮ���ռ�����ʱ���Թ۲쵽______Ϊ���������ı���
���������ַ����У�______���ռ�����������������
�������ſ������ռ���������Ũ��ֻ��80%���ҵ�ԭ������_____��
A���������ܶ��Դ��ڿ������ܶ�
B�����ȸ�����ع������������Ũ��ֻ��80%����
C�����۲쵽������ľ����ȼʱ������ƿ�ڻ��п���
D�����������뼯��ƿʱ��ƿ�ڿ����������������ɢ