题目内容
小敏在实验室发现一块长期暴露在空气中的氢氧化钠固体,为了检验它是否完全变质,进行了如下实验.
(1)请写出氢氧化钠变质的化学反应方程式 .
(2)表格中加入足量BaCl2的目的是 .
| 实验操作 | 实验现象 | 结论 |
| (1)取固体于试管中,加入适量蒸馏水制成溶液备用, | ||
| (2)取少量样品于试管中,滴加少量 | 产生大量气泡, | 说明已变质 |
| (3)取少量样品,滴加足量的BaCl2溶液,再滴加少量 | ①如果溶液变红, ②如果溶液 | 说明氢氧化钠 说明氢氧化钠完全变质 |
(2)表格中加入足量BaCl2的目的是
考点:药品是否变质的探究,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的分离、除杂、提纯与共存问题
分析:根据已有的知识进行分析,物质露置在空气的情况是不变质、部分变质或是全部变质,氢氧化钠变质是因为与二氧化碳发生反应生成了碳酸钠,要证明变质就是证明含有碳酸钠,可以使用与钙离子或钡离子结合产生沉淀的方法,要证明氢氧化钠的存在,需要除去碳酸钠,但是加入的试剂不能反应生成氢氧化钠,否则会对反应造成干扰.
解答:解:小敏在实验室发现一块长期暴露在空气中的氢氧化钠固体,物质露置在空气的情况是不变质、部分变质或是全部变质,氢氧化钠变质是因为与二氧化碳发生反应生成了碳酸钠,要证明变质就是证明含有碳酸钠,可以使用滴加稀盐酸产生二氧化碳气泡的方法,要证明氢氧化钠的存在,需要除去碳酸钠,但是加入的试剂BaCl2溶液 不能反应生成氢氧化钠,为了检验它是否完全变质,滴加酚酞溶液,根据溶液的变色情况,分析判断氢氧化钠的变质情况,根据以上分析完成表格:
(1)氢氧化钠变质的化学反应方程式:CO2+2NaOH=Na2CO3+H2O.
(2)表格中加入足量BaCl2的目的是除尽溶液中的碳酸钠,避免对检验氢氧化钠造成干扰.故答案为:
(1)CO2+2NaOH=Na2CO3+H2O;
(2)除尽溶液中的碳酸钠,避免对检验氢氧化钠造成干扰.
| 实验操作 | 实验现象 | 结论 |
| (1)取固体于试管中,加入适量蒸馏水制成溶液备用, | ||
| (2)取少量样品于试管中,滴加少量稀盐酸, | 产生大量气泡, | 说明已变质 |
| (3)取少量样品,滴加足量的BaCl2溶液,再滴加少量酚酞溶液, | ①如果溶液变红, ②如果溶液不变色. | 说明氢氧化钠部分变质; 说明氢氧化钠完全变质 |
(2)表格中加入足量BaCl2的目的是除尽溶液中的碳酸钠,避免对检验氢氧化钠造成干扰.故答案为:
| 实验操作 | 实验现象 | 结论 |
| (1)取固体于试管中,加入适量蒸馏水制成溶液备用, | ||
| (2)取少量样品于试管中,滴加少量稀盐酸, | 产生大量气泡, | 说明已变质 |
| (3)取少量样品,滴加足量的BaCl2溶液,再滴加少量酚酞溶液, | ①如果溶液变红, ②如果溶液不变色. | 说明氢氧化钠部分变质; 说明氢氧化钠完全变质 |
(2)除尽溶液中的碳酸钠,避免对检验氢氧化钠造成干扰.
点评:熟练掌握氢氧化钠、碳酸钠的性质,题目通过药品是否变质的探究培养了学生的实验探究能力,

练习册系列答案
相关题目
 已知A~G是我们熟悉的物质,其中A、E、F、G都是单质,B、C、D都是氧化物,A、B、C都是空气的成分,E是红色固体,F是目前产量最高的金属,它们之间有如图所示的反应与转化关系(图中“-”表示两种物质能反应,“→”表示转化关系).
已知A~G是我们熟悉的物质,其中A、E、F、G都是单质,B、C、D都是氧化物,A、B、C都是空气的成分,E是红色固体,F是目前产量最高的金属,它们之间有如图所示的反应与转化关系(图中“-”表示两种物质能反应,“→”表示转化关系).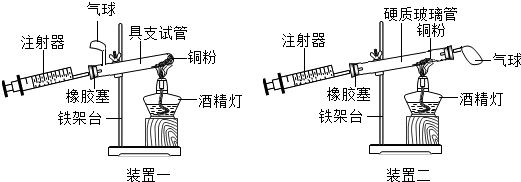
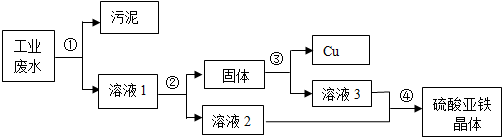
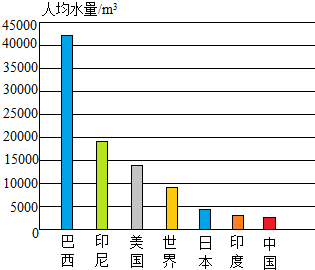 如图所示为世界人均水量和一些国家的人均水量,
如图所示为世界人均水量和一些国家的人均水量, 如图是某种胃药的部分标识.胃药中所含的物质能中和胃里过多的胃酸.某患者按标识上的服用方法服药,服药后病情好转.计算:
如图是某种胃药的部分标识.胃药中所含的物质能中和胃里过多的胃酸.某患者按标识上的服用方法服药,服药后病情好转.计算: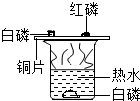 探究燃烧条件的实验装置如图所示.
探究燃烧条件的实验装置如图所示.