题目内容
取8g氧化铜与100g稀硫酸恰好完全反应后得到蓝色溶液,试计算:
(1)反应后所得溶液中溶质的质量是多少?
(2)求稀硫酸中溶质的质量分数?
(1)反应后所得溶液中溶质的质量是多少?
(2)求稀硫酸中溶质的质量分数?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据氧化铜的质量和反应的化学方程式求出生成的硫酸铜的质量;
(2)根据氧化铜的质量和反应的化学方程式求出稀硫酸中溶质的质量,进而求质量分数.
(2)根据氧化铜的质量和反应的化学方程式求出稀硫酸中溶质的质量,进而求质量分数.
解答:解:设反应后所得溶液中溶质的质量为x,稀硫酸中溶质的质量为y
CuO+H2SO4=CuSO4+H2O
80 98 160
8g y x
=
=
x=16g,y=9.8g
稀硫酸中溶质的质量分数:
×100%=9.8%.
答:(1)反应后所得溶液中溶质的质量为16g;
(2)稀硫酸中溶质的质量分数为9.8%.
CuO+H2SO4=CuSO4+H2O
80 98 160
8g y x
| 80 |
| 8g |
| 98 |
| y |
| 160 |
| x |
x=16g,y=9.8g
稀硫酸中溶质的质量分数:
| 9.8g |
| 100g |
答:(1)反应后所得溶液中溶质的质量为16g;
(2)稀硫酸中溶质的质量分数为9.8%.
点评:本题主要考查根据化学方程式的基本计算,注意计算过程要规范.

练习册系列答案
相关题目
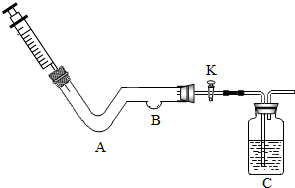 某化学小组同学利用如图所示装置进行实验.
某化学小组同学利用如图所示装置进行实验.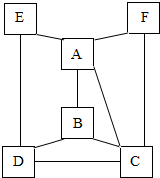 如图中有A、B、C、D、E、F六种物质,它们是氢氧化钙、稀硫酸、硝酸钡、碳酸钠、氯化锌五种溶液和单质镁,凡是用直线相连的两种物质间均可发生化学反应.试推断:
如图中有A、B、C、D、E、F六种物质,它们是氢氧化钙、稀硫酸、硝酸钡、碳酸钠、氯化锌五种溶液和单质镁,凡是用直线相连的两种物质间均可发生化学反应.试推断: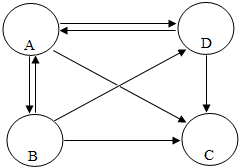 如图所示,箭头表示各物质间的转换关系,箭头指向的为生成物,部分反应物或生成物已略去.现有氯化钠溶液、碳酸钠溶液、氢氧化钠溶液和硫酸钠溶液,请回答下列问题:
如图所示,箭头表示各物质间的转换关系,箭头指向的为生成物,部分反应物或生成物已略去.现有氯化钠溶液、碳酸钠溶液、氢氧化钠溶液和硫酸钠溶液,请回答下列问题: