题目内容
【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
①为探究催化剂的种类对氯酸钾分解速率的影响,甲设计以下对比实验:
编号 | 实验药品 | 分解温度(℃) |
Ⅰ | 3.0gKClO3与1.0gMnO2均匀混合加热 | 350 |
Ⅱ | xgKClO3与1.0gCuO均匀混合加热 | 370 |
Ⅰ中反应的化学方程式是_______;
Ⅱ中x的值应为________。
[实验结论]实验所用两种金属氧化物中,催化效果最好的是_______。
②乙探究了影响双氧水分解速率的某种因素,实验数据记录如下:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
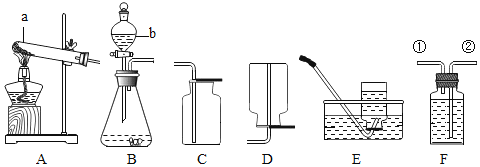
本实验中,测量O2体积的装置是______(填编号)。
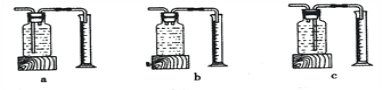
[实验结论]在相同条件下,_______,双氧水分解得越快。
[反思]丙用如图装置进行实验,通过比较_____也能达到实验目的。

【答案】2KClO3![]() 2KCl+3O2↑ 3.0 MnO2 C 过氧化氢浓度越大 相同时间天平读数差值大小
2KCl+3O2↑ 3.0 MnO2 C 过氧化氢浓度越大 相同时间天平读数差值大小
【解析】
①
Ⅰ实验中氯酸钾在二氧化锰的催化下分解成氯化钾和氧气,化学方程式故填2KClO3 ![]() 2KCl+3O2↑;
2KCl+3O2↑;
Ⅱ通过控制氯酸钾的质量相等才能比较出二氧化锰和氧化铜的催化效果,所以氯酸钾的质量也为3.0g,故填3.0;
[实验结论]
相同条件下用二氧化锰催化氯酸钾在350℃时分解,而用氧化铜催化氯酸钾要在370℃时才能分解,催化所需温度越低的效果越好,故填MnO2(二氧化锰);
②使用万用瓶排水法集气时,短管进气长管排水,故填C;
[实验结论]
从表中实验数据可知在相同条件下,双氧水的浓度越大,产生氧气的速率越快,故填双氧水浓度越大;
[反思]
过氧化氢和二氧化锰的反应放在电子天平上,由于反应生成氧气且容器敞口,所以容器中剩余物质的质量会减轻,减轻的质量就是生成的氧气的质量,根据相同时间内,电子天平读数的差值大小也可以达到实验目的,故填相同时间天平读数差值大小。

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
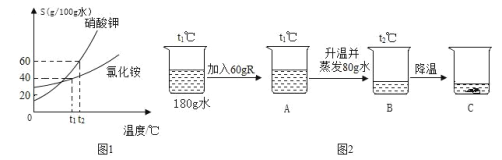
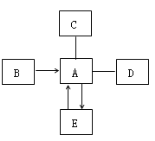
蓝天教育暑假优化学习系列答案【题目】如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
温度(℃) | t1 | t2 |
KNO3的溶解度(g/100g水) | 60 | 90 |
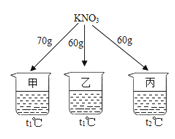
A. 乙、丙溶液中溶质质量相等
B. 乙升温至t2℃,溶液质量增加
C. 甲、乙混合后为t1℃的不饱和溶液
D. 丙降温至t1℃,有晶体析出