题目内容
(4分)有三种无标签的白色固体,已知它们分别是硝酸铵、氯化钾和硫酸钠,请设计方案鉴别它们,完成下表:
| 操 作 | 预期现象与结论 |
| | |
| | |
(每空1分 共4分)有三种无标签的白色固体,已知它们分别是硝酸铵、氯化钾和硫酸钠,请设计方案鉴别它们,完成下表:
只要合理都给分。如取少量固体分别与熟石灰混合,有刺激性气味气体产生的为硝酸铵,再去区别后两种等。
| 操 作 | 预期现象与结论 |
| 分别取样溶于少量水中, | 温度降低的(或变凉的)原固体为硝酸铵,其余两种(或无明显变化的)为氯化钾或硫酸钠 |
| 往上述无变化的两种溶液中滴加BaCl2或Ba(NO3)2溶液, | 产生白色浑浊的原固体为硫酸钠,无沉淀的原固体为氯化钾 |
分析:根据硝酸铵溶于水时溶液的温度会降低,硫酸根离子会与钡离子生成白色沉淀进行分析.
解答:解:可以先加水溶解根据溶液温度的变化鉴别出硝酸铵,然后再利用硝酸钡鉴别出硫酸钠,故答案为:
解答:解:可以先加水溶解根据溶液温度的变化鉴别出硝酸铵,然后再利用硝酸钡鉴别出硫酸钠,故答案为:
| 操作 | 预期现象与结论 |
| 分别取样溶于少量水中, | 温度降低的原固体为硝酸铵,无明显变化的为氯化钾或硫酸钠 |
| 往上述无变化的两种溶液中滴加Ba(NO3)2溶液, | 产生白色浑浊的原固体为硫酸钠,无沉淀的原固体为氯化钾 |

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
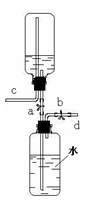
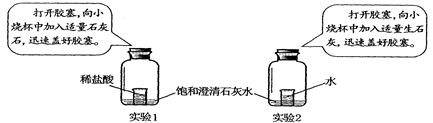


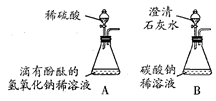 ②CaSO4微溶,但在稀溶液中看作可溶,其水溶液呈中性.)
②CaSO4微溶,但在稀溶液中看作可溶,其水溶液呈中性.)