题目内容
某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把40g稀盐酸(氯化氢的水溶液)分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶解于水),充分反应后经过过滤、干燥等操作,最后称量,得实验数据如下:
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入10g | 3.0g |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.2g |
| 第四次加入10g | 1.2g |
(2)石灰石样品中碳酸钙的纯度是多少?
(3)现要高温煅烧制取生石灰(CaO)56t,需要上述这种纯度的石灰石质量为多少?(CaCO3
 CaO+CO2↑)
CaO+CO2↑)
解:(1)由4、5次实验的数据可知最后剩余的1.2克为杂质质量;
(2)石灰石样品中碳酸钙的纯度是: ×100%=70%;
×100%=70%;
(3)设现要高温煅烧制取生石灰56t,需要上述这种纯度的石灰石质量为X
CaCO3 CaO+CO2↑
CaO+CO2↑
100 56
X×70% 56t
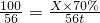 解得:X=142.9t
解得:X=142.9t
答:(1)4g石灰石样品中,有杂质1.2克;(2)石灰石样品中碳酸钙的纯度是70%;(3)现要高温煅烧制取生石灰(CaO)56t,需要上述这种纯度的石灰石质量为142.9t.
分析:(1)根据实验3、4可知剩余固体的质量是杂质的质量;
(2)由杂质的质量可计算出石灰石中碳酸钙的质量,由碳酸钙的质量可计算出石灰石中碳酸钙的质量分数;
(3)根据高温煅烧制取生石灰的反应,由生石灰的质量求出这种纯度的石灰石质量.
点评:此题是对化学方程式计算的综合考查题,根据质量守恒定律,反应后所得溶液的质量=碳酸钙的质量+所加稀盐酸的总质量-放出二氧化碳气体的质量是解题的关键.
(2)石灰石样品中碳酸钙的纯度是:
 ×100%=70%;
×100%=70%;(3)设现要高温煅烧制取生石灰56t,需要上述这种纯度的石灰石质量为X
CaCO3
 CaO+CO2↑
CaO+CO2↑100 56
X×70% 56t
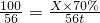 解得:X=142.9t
解得:X=142.9t答:(1)4g石灰石样品中,有杂质1.2克;(2)石灰石样品中碳酸钙的纯度是70%;(3)现要高温煅烧制取生石灰(CaO)56t,需要上述这种纯度的石灰石质量为142.9t.
分析:(1)根据实验3、4可知剩余固体的质量是杂质的质量;
(2)由杂质的质量可计算出石灰石中碳酸钙的质量,由碳酸钙的质量可计算出石灰石中碳酸钙的质量分数;
(3)根据高温煅烧制取生石灰的反应,由生石灰的质量求出这种纯度的石灰石质量.
点评:此题是对化学方程式计算的综合考查题,根据质量守恒定律,反应后所得溶液的质量=碳酸钙的质量+所加稀盐酸的总质量-放出二氧化碳气体的质量是解题的关键.

练习册系列答案
相关题目
某化学兴趣小组为了分析生铁中铁的含量,进行了实验研究,即取60g经粉碎后的生铁,把800稀硫酸分4次加入到该样品中,测得数据记录如下表:
(说明:生铁中杂质不溶于水,也不与硫酸反应.)
(1)第2次测得剩余固体质量为15.2g,其成分为 .
A.铁 B.铁和碳 C.碳
(2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)
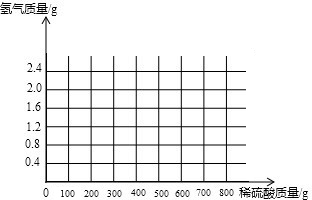
(3)计算所用稀硫酸的溶质质量分数为多少?(写出计算过程,结果保留到小数点后一位)并画出反应生成的氢气质量与加入稀硫酸质量的关系图.
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量(g) | 200 | 200 | 200 | 200 |
| 剩余固体质量(g) | 37.6 | 15.2 | 4 | 4 |

(说明:生铁中杂质不溶于水,也不与硫酸反应.)
(1)第2次测得剩余固体质量为15.2g,其成分为
A.铁 B.铁和碳 C.碳
(2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)
(3)计算所用稀硫酸的溶质质量分数为多少?(写出计算过程,结果保留到小数点后一位)并画出反应生成的氢气质量与加入稀硫酸质量的关系图.
我市某地盛产石灰石,其中含有不溶于盐酸的杂质.某化学兴趣小组为了测定石灰石中碳酸钙的含量,取10.0g石灰石样品,经粉碎后全部放入烧杯中,并加入足量的稀盐酸,烧杯及所盛物质的总质量为80.0g.反应过程中测得烧杯及所盛物质的质量与相应时间记录如下表:
试计算:(1)反应结束后,共放出多少克的二氧化碳?
(2)该石灰石样品中碳酸钙的质量分数是多少?
| 反应时间/分 | 0 | 2 | 4 | 6 | 8 | 10 |
| 烧杯及所盛物质质量/克 | 80.0 | 79.0 | 78.3 | 77.9 | 77.8 | 77.8 |
(2)该石灰石样品中碳酸钙的质量分数是多少?
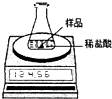 某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验.实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止.测得反应前后的有关质量如表:
某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验.实验装置如图所示,称取研细的2.60g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止.测得反应前后的有关质量如表: