��Ŀ����
����Ŀ��ij��ȤС��������ͼ��ʾװ�ý����������ȡʵ�飬��ش���������
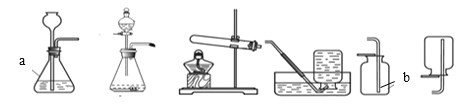
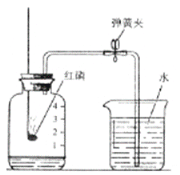
�� д����ŵ��������ƣ�a _____ ��b _________
�� ��A��ȣ�B��Ϊ��ȡ�����ķ���װ�ã��ŵ���_________ ��
�� ����Dװ���ռ������������ܿ�����ʢ��ˮ�ļ���ƿ�п�ʼ�ռ�����������ʱ����_____��������______������ʱ��˵������������
�� ��������غͶ������̵Ļ����õ�0.03mol��������������Ҫ���ٿ�����ء������ݻ�ѧ����ʽ��ʽ���㣩___________
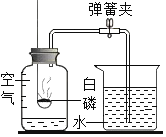
�� ʵ���ҿɲ����Ȼ�����������ƹ��干�����ư����������ͼװ����ѡ��ʵ�����ư����ķ���װ��_____�������ţ�
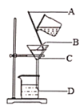
�� ʵ������˫��ˮ�Ͷ����������Ƶ������ķ���װ����_______�����ţ�дһ�֣�����ѧ����ʽ��__________��
���𰸡���ƿ ����ƿ �ܹ����Ƽ���Һ������ʣ��Ա�õ�ƽ���������������ɣ� ������������ʱ ����ƿ��ˮ�ž��������ݴ�ƿ�����������ð���� 2.45g C A��B H2O2 ![]() H2O+O2
H2O+O2
��������
������a����������ƿ��������ƿ��
����b�������Ǽ���ƿ�������ƿ��
�� ��A��ȣ�B��Ϊ��ȡ�����ķ���װ�þ��е��ŵ��ǣ��ܹ����Ƽ���Һ������ʣ��Ա�õ�ƽ�������������ܹ����Ƽ���Һ������ʣ��Ա�õ�ƽ���������������ɣ���
������ˮ���ռ�����ʱ����ʼ�ռ����������ʱ���ǵ��ܿڳ�����������ʱ������ܿڳ�����������ʱ��
��ˮ���ռ������ռ����ı�־�Ǽ���ƿ��ˮ�ž��������ݴ�ƿ�������ݳ���ð�����������ƿ��ˮ�ž��������ݴ�ƿ�������ݳ���ð������
���⣺0.03mol����������Ϊ0.03mol��32g/ mol=0.96g
����Ҫ����ص�����Ϊx
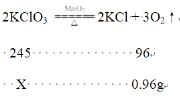
245��96 = x��0.96g
X = 2.45g
����Ҫ����ص�����Ϊ2.45g.
�� ʵ���ҿɲ����Ȼ�����������ƹ��干�����ư�����Ӧѡ��������ȷ���װ�ã�����C��
�� ʵ������˫��ˮ�Ͷ����������Ƶ������ǹ����Һ�峣�·�Ӧ�������壬Ӧѡ���Һ���·���װ�ã�����A��B��
���������ڶ��������������������·�Ӧ����ˮ���������ʻ�ѧ����ʽдΪ��2H2O2![]() 2H2O + O2����
2H2O + O2����

����Ŀ��ʵ��С��Թ���������ȡ������Ӱ�췴Ӧ���ʵ����ؽ���̽����
[�������] ��Щ���ؿ���Ӱ��÷�Ӧ�ķ�Ӧ���ʣ�
[��������] С��ͬѧ��H2O2��Һ��Ũ�ȿ���Ӱ��÷�Ӧ�ķ�Ӧ���ʣ�
С��ͬѧ��������MnO2������������Ӱ��÷�Ӧ�ķ�Ӧ���ʡ���
[ʵ����֤]
��1��Ϊ��̽��������������ͬʱH2O2��ҺŨ�ȶԷ�Ӧ���ʵ�Ӱ�죬С��ͬѧ��ʵ���ǣ�ÿ�ξ�ȡ10mL30%��H2O2��Һ��Ȼ����ɲ�ͬŨ�ȵ���Һ������ͬ�¶��¼��������MnO2����ʵ�飬�ⶨ�����ռ���100mL����ʱ���õ�ʱ�䣬��¼�������£�
ʵ����� | 1 | 2 | 3 | 4 | 5 |
H2O2��ҺŨ�� | 1% | 5% | 15% | 25% | 30% |
����ʱ�䣨�룩 | 660 | 205 | 25 | 4 | 3 |
ͨ���ϱ�ʵ�����ݷ����ɵõ��Ľ����ǣ�������������ͬ������£�_____Խ��Ӧ����Խ_____��
��2��Ϊ��̽��������������ͬʱ������MnO2���������Է�Ӧ���ʵ�Ӱ�죬С��ͬѧ��ʵ���ǣ�ÿ�ξ���30mL10%��H202��Һ����ͬ�¶��½���ʵ�飬���ò�ͬ��MnO2��ĩ���������ⶨ�����ռ���100mL����ʱ���õ�ʱ�䣬��ͼ���£�
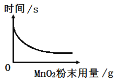
�ٸ÷�Ӧ�Ļ�ѧ����ʽΪ��__________
��ͨ����ͼʵ�����ݷ����ɵõ��Ľ����ǣ� ________
��3��С��ͬѧ��Ϊ��������Ҳ���ܻ�Ӱ��÷�Ӧ�����ʡ�
С��ͬѧ��ʵ���ǣ�ÿ�ξ�ȡ10mL30%��H2O2��Һ��Ȼ�����һ��Ũ�ȵ���Һ����ʵ�顣
ʵ����� | 1 | 2 | 3 | 4 | 5 |
H2O2��ҺŨ�� | �� | 10% | 10% | 10% | 10% |
�������̷�ĩ����/g | 0��2 | 0��2 | �� | 0��2 | 0��2 |
�¶�/�� | 20 | 30 | 40 | 50 | 60 |
�������� |
��д�������ݣ��� ___________ �� ___________��
��С��ͬѧʵ��̽����Ŀ���� _________��
�����´������ݺ�������_____________
A���ⶨ����ʵ���ռ���100mL����ʱ���õ�ʱ��
B���ⶨ����ʵ����30s���ռ������������
C���ⶨ����ʵ����ȫ��Ӧʱ�ռ������������
����Ŀ�����������������������й㷺Ӧ�á�ʵ��С��Թ��������ijЩ���ʽ����о���
���ȶ���
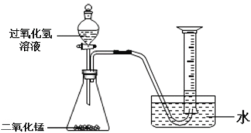
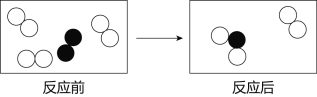
��1������ͼ��ʾ����ʵ�飬��������ֽ�Ļ�ѧ����ʽΪ______��
��2��������ˮ���ռ�O2��ԭ����______��
��3��̽���¶ȶԹ�������ֽ����ʵ�Ӱ�졣
ͬѧ�ǽ��������µ�ʵ�飬ʵ���������±���
ʵ����� | �� | �� | �� |
H2O2��Һ��Ũ�� % | 30 | 30 | 30 |
H2O2��Һ�����/mL | 6 | 6 | 6 |
�¶�/�� | 20 | 35 | 55 |
MnO2������/g | 0 | 0 | 0 |
�ռ�O2�����/mL | 0 | 1.9 | 7.8 |
��Ӧʱ�� | 40 min | 40 min | 40 min |
�ɴ˵ó��Ľ�����______��
��ʴ��
���������ϣ�H2O2��Һ�и�ʴ�ԡ�
������ʵ�飩
ͬѧ����ͭƬ���ʵ����֤H2O2��Һ�ĸ�ʴ�ԡ�������ʵ����H2O2��Һ��ϡ��������Ũ�Ⱦ���ͬ��
��ͭƬ�ֱ������3����Һ�н���ʵ�飬���±���
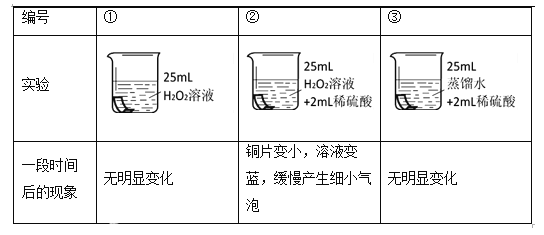
����������ۣ�
��4��ʵ��ٵ�������______��
��5����˵��ͭƬ����ʴ��H2O2��Һ��ϡ������йص�ʵ������______��
��6��ͭƬ����ʴ�ķ�Ӧ���£���ȫ�÷�Ӧ�Ļ�ѧ����ʽ��Cu + H2O2+ H2SO4=== CuSO4 +��_______/p>