题目内容
【题目】实验小组对过氧化氢制取氧气中影响反应速率的因素进行探究。
[提出问题] 哪些因素可能影响该反应的反应速率?
[作出猜想] 小芳同学:H2O2溶液的浓度可能影响该反应的反应速率;
小华同学:催化剂(MnO2)的用量可能影响该反应的反应速率……
[实验验证]
(1)为了探究在其他条件相同时H2O2溶液浓度对反应速率的影响,小芳同学的实验是:每次均取10mL30%的H2O2溶液,然后配成不同浓度的溶液,在相同温度下加入等质量MnO2进行实验,测定各次收集到100mL氧气时所用的时间,记录数据如下:
实验次序 | 1 | 2 | 3 | 4 | 5 |
H2O2溶液浓度 | 1% | 5% | 15% | 25% | 30% |
所用时间(秒) | 660 | 205 | 25 | 4 | 3 |
通过上表实验数据分析可得到的结论是:在其他条件相同的情况下,_____越大,反应速率越_____。
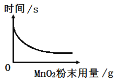
(2)为了探究在其他条件相同时催化剂(MnO2)的用量对反应速率的影响,小华同学的实验是:每次均用30mL10%的H202溶液在相同温度下进行实验,采用不同量MnO2粉末做催化剂,测定各次收集到100mL氧气时所用的时间,绘图如下:
①该反应的化学方程式为:__________
②通过如图实验数据分析可得到的结论是: ________
(3)小明同学认为其他条件也可能会影响该反应的速率。
小明同学的实验是:每次均取10mL30%的H2O2溶液,然后配成一定浓度的溶液进行实验。
实验次序 | 1 | 2 | 3 | 4 | 5 |
H2O2溶液浓度 | ① | 10% | 10% | 10% | 10% |
二氧化锰粉末用量/g | 0.2 | 0.2 | ② | 0.2 | 0.2 |
温度/℃ | 20 | 30 | 40 | 50 | 60 |
待测数据 |
填写表中数据:① ___________ ② ___________。
③小明同学实验探究的目的是 _________。
④以下待测数据合理的是_____________
A.测定各次实验收集到100mL氧气时所用的时间
B.测定各次实验在30s里收集到的氧气体积
C.测定各次实验完全反应时收集到的氧气体积
【答案】H2O2溶液浓度; 大 2H2O2 MnO22H2O+ O2 ↑ 在其他条件相同的情况下,在一定范围内,催化剂(MnO2)的用量越大,反应速率越大 10% ; 0.2 探究在其他条件相同时,温度对反应速率的影响 AB
【解析】
(1)比较表格中的数据在其他条件都相同时,可以得出过氧化氢的浓度大的收集100mL气体所用时间最短,所以:在催化剂、温度等相同的条件下,H2O2溶液的浓度越大,反应速率越大;
(2)①过氧化氢在二氧化锰催化作用下生成水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+ O2 ↑;
2H2O+ O2 ↑;
②比较表格中的数据在其他条件都相同时,可以得出二氧化锰的用的质量越大,收集500mL气体所用的时间越短,在过氧化氢溶液浓度、温度等相同的条件下,MnO2的用量越大(在一定范围内),反应速率越大;
(3)① 由实验2-5H2O2溶液浓度为10%分析,可知实验1H2O2溶液浓度应为10%;
②由实验1、2、4、5二氧化锰粉末用量为0.2g分析,可知实验3二氧化锰粉末用量应为0.2g;
③分析表中数据可知,小明同学实验探究的目的是:探究在其他条件相同时,温度对反应速率的影响;
④A、测定各次实验收集到100mL氧气时所用的时间,可以探究温度对反应速率的影响;B、测定各次实验在30s里收集到的氧气体积,可以探究温度对反应速率的影响;C、测定各次实验完全反应时收集到的氧气体积,不可以探究温度对反应速率的影响。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案