题目内容
【题目】硫酸铜晶体(CuSO4﹒5H2O)常用于印染的媒染剂,农业和渔业的杀虫剂、工业镀铜等。
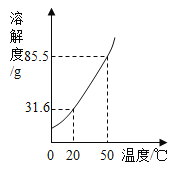
[物质制备]某兴趣小组同学查找到以辉铜矿(主要成分是硫化亚铜,化学式为Cu2S) 为主要原料制备硫酸铜晶体的工业生产过程:
[资料1 ]硫化亚铜(Cu2S)高温时能与空气中的氧气反应生成氧化铜和二氧化硫气体。
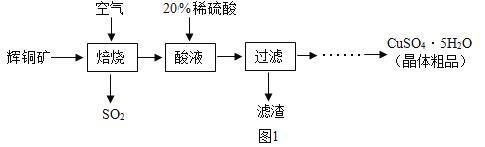
(1)Cu2S中铜元素的化合价为______________。
(2)焙烧过程中为了让辉铜矿充分反应,可以采取的措施是______________。
(3),上述“酸溶”过程中发生反应的化学方程式是______________。上述流程中产生的SO2可用于工业上生产硫酸。
(4)制得硫酸铜晶体粗品的过程是:将滤液经蒸发浓缩、降温结晶、_________、洗涤、 低温干燥而获得。
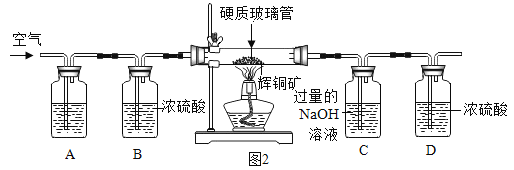
[含量测定]该兴趣小组的同学为测定某辉铜矿中硫元素的含量,进行了如下的实验探究。(假设每步反应均完全,不考虑装置内原有空气对测定结果的影响)。该实验小组设计了下列装置,取6g辉铜矿样品,放入硬质玻璃管中。
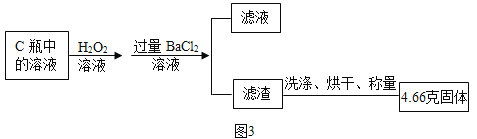
充分反应后,取C瓶中的溶液进行了如下图处理:
[资料Ⅱ]亚硫酸钠(Na2SO3) 与过氧化氢反应能生成硫酸钠和水。
[问题讨论] (5)图2装置中A瓶内.所盛的试剂是NaOH溶液,其作用是______________;C瓶中NaOH溶液的作用是______________。
(6)图3实验过程中必须对滤渣进行洗涤,证明滤渣洗净所用试剂是_____________溶液,若缺少洗涤操作则会使测得的硫化亚铜的含量_____________(选填“偏大”、“偏小”或“不变”)。
(7)图3实验过程中,加入过量BaCl2溶液时发生反应的化学方程式为______________;该辉铜矿中硫元素的质量分数为______________。(假设辉铜矿中只有Cu2S 含有S元素,且转化过程中无硫元素的损失)
【答案】+1 将辉铜矿研成粉末 ![]() 过滤 吸收空气中的二氧化碳,防止测得二氧化硫的质量偏大 吸收硬质玻璃管内生成的二氧化硫 硫酸钠 偏大
过滤 吸收空气中的二氧化碳,防止测得二氧化硫的质量偏大 吸收硬质玻璃管内生成的二氧化硫 硫酸钠 偏大 ![]() 16%
16%
【解析】
(1)硫元素通常为-2价,设Cu2S中铜元素的化合价为x,根据化合物中正、负化合价的代数和为零,可得:2x+(-2)=0,x=+1;
(2)焙烧过程中为了让辉铜矿充分反应,可以采取的措施是:将辉铜矿研成粉末,可以增大反应物之间接触面积;
(3)“酸溶”过程为氧化铜和稀硫酸反应生成硫酸铜和水,该反应的化学方程式为:![]() ;
;
(4)制得硫酸铜晶体粗品的过程是:将滤液经蒸发浓缩、降温结晶、过滤、洗涤、 低温干燥而获得;
问题讨论:(5)图2装置中A瓶内所盛的试剂是NaOH溶液,其作用是吸收空气中的二氧化碳,防止测得二氧化硫的质量偏大;
C瓶中NaOH溶液的作用是:吸收硬质玻璃管内生成的二氧化硫;
(6)C瓶中的溶液为氢氧化钠和二氧化硫反应生成的亚硫酸钠,亚硫酸钠能与过氧化氢反应生成硫酸钠和水,加过量氯化钡溶液,氯化钡与硫酸钠反应生成硫酸钡沉淀和氯化钠,故滤渣为硫酸钡沉淀,滤液中的溶质为氯化钡和氯化钠,证明滤渣洗净所用试剂是硫酸钠溶液,硫酸钠能与氯化钡反应生成硫酸钡沉淀;
若缺少洗涤操作,会导致测定的沉淀质量偏大,则会使测得的硫化亚铜的含量偏大;
(7)图3实验过程中,加入过量BaCl2溶液,氯化钡与硫酸钠反应生成硫酸钡沉淀和氯化钠,发生反应的化学方程式为:![]()
图2、图3中发生反应的化学方程式为:
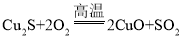 ,
,![]() ,
,![]() ;
;![]() ,由化学方程式可知,硫化亚铜中的硫元素全部转移到了硫酸钡沉淀中,根据质量守恒定律,化学反应前后,原子的种类、数目、质量不变,故硫元素的质量为:
,由化学方程式可知,硫化亚铜中的硫元素全部转移到了硫酸钡沉淀中,根据质量守恒定律,化学反应前后,原子的种类、数目、质量不变,故硫元素的质量为:![]() ,辉铜矿中硫元素的质量分数为:
,辉铜矿中硫元素的质量分数为:![]() 。
。

【题目】今年“五·一”假期,小丽随爸爸到乡下省亲,期间看到许多漂亮的大理石,于是好带了一些回来,想去学校实验室测定这此大理石中CaCO3的含量。他称取了20克大理石样品置于烧杯中,然后将250g稀盐酸分成五等份,依次加入烧杯充分反应,记录有关实验数据如下表所示(大理石中其他分均不溶于水,也不参与化学反应)。
加入次数 | 一 | 二 | 三 | 四 | 五 |
加入稀盐酸的质量 | 50 | 50 | 50 | 50 | 50 |
烧杯中剩余固体的质量 | 15 | 10 | 5 | 5 | m |
试求:(1)m的值应为_____;
(2)实验中大理石样品所含CaCO3的质量分数?_____
(3)实验中所用稀盐酸的溶质质量分数?_____