题目内容
【题目】拉瓦锡曾经做了这样一个实验:让水蒸气通过一根烧红的枪管,生成了一种气体。同学们对这个实验很感兴趣,设计了如图所示的装置进行探究:在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水和铁反应)。
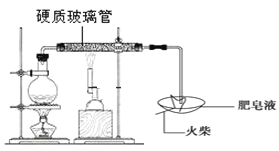
(1)反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当听到有爆鸣声时,说明“铁与水蒸气”能够进行反应,生成_____(写化学式)。
(2)实验中石棉绒的作用是_______。
(3)探究玻璃管中剩余固体成分是什么?
(查阅资料)1.常见铁的氧化物的性质
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
与稀硫酸反应 | 生成FeSO4 | 生成Fe2(SO4)3 | 生成FeSO4 、Fe2(SO4)3 |
2.铁可与硫酸铁溶液反应生成硫酸亚铁。
(初步验证)玻璃管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_______。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
将玻璃管中的剩余固体取出,放入试管中,加入过量的稀硫酸。 | 有气泡产生 | ______ |
(反思与交流)往剩余固体中加入过量的稀硫酸后,若无气体产生,你_______(填“能”或“不能”)确定剩余固体成分,原因是________。
【答案】H2 增大铁粉与水蒸气的接触面 Fe3O4 剩余固体是Fe和Fe3O4 不能 四氧化三铁与稀硫酸反应生成硫酸铁,硫酸铁会与铁反应生成硫酸亚铁,无法观察到气泡,不能确定铁的存在
【解析】
(1)由实验现象“用点燃的火柴靠近肥皂泡,听到有爆鸣声”可知,反应后生成了氢气,其化学式为H2,故填H2。
(2)实验中石棉绒增大了铁粉与水蒸气的接触面,使反应的速率加快,故填增大了铁粉与水蒸气的接触面。
(3)由“玻璃管中剩余固体为黑色,能全部被磁铁吸引”可猜想反应后产生的固体为Fe3O4,故填Fe3O4;
由将玻璃管中的剩余固体取出,放入试管中,加入过量的稀硫酸,有气泡产生,说明剩余固体中含有铁,则剩余固体为Fe和Fe3O4,故填剩余固体为Fe和Fe3O4;
往剩余固体中加入过量的稀硫酸后,若无气体产生,则不能确定剩余固体成分,故填不能;
不能确定剩余固体成分的理由是四氧化三铁与稀硫酸反应生成硫酸铁,硫酸铁会与铁反应生成硫酸亚铁,无法观察到气泡,不能确定铁的存在,故填四氧化三铁与稀硫酸反应生成硫酸铁,硫酸铁会与铁反应生成硫酸亚铁,无法观察到气泡,不能确定铁的存在。

 口算题卡北京妇女儿童出版社系列答案
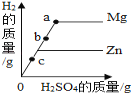
口算题卡北京妇女儿童出版社系列答案【题目】在一密闭容器中,物质X不完全燃烧时可以产生一氧化碳、二氧化碳和水。依据下表数据分析得出的结论中,正确的是
物质 | X | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
反应前质量/g | 6.6 | 8.8 | 0 | 0 | 0 |
反应后质量/g | 2 | 0 | 6.6 | 5.4 | a |
A. X中碳元素的质量分数为52.2% B. X中只含有C、H两种元素
C. 表中a的值为3.4 D. 无法确定X中是否含有氧元素
【题目】化学与生活、生产密切相关。
(1)我国首架大型客机C919中使用了大量的铝镁合金,铝制品在空气中不易被腐蚀,具有“自我保护”能力,其原因是_____(用化学方程式表示)。
(2)铝、铜、银是日常生活中接触到的三种金属。同学甲设计了如下三个实验来验证它们的金属活动性强弱:① 铝、硝酸银溶液;②铜、硫酸铝溶液;③铜、硝酸银溶液。同学乙认为这一方案中实验 ______(填“①”、“②”、“③”)可以不做,也能验证三个金属的活动性强弱。请写出实验③中的实验现象______。
(3)中国南海海底有大量的可燃冰(CH4·nH2O)。
① 可燃冰中,水分子形成一种空间笼状结构,甲烷和少量N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于________(选填“纯净物”或“混合物”)。
②甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | 一氧化碳 |
反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | 未测 |
根据表格中数据,请完成甲烷在一定量的氧气中燃烧的化学方程式 _______。
(4)某工厂利用废硫酸与废铁屑反应制取硫酸亚铁。现制得FeSO4 1.52 t,需要铁的质量至少是多少?(在答题卡上写出计算过程)_______
【题目】某化学兴趣小组在探究物质燃烧条件时,做了如下实验:
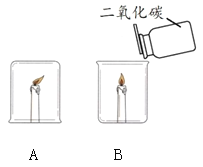
同学们发现两支蜡烛都熄灭了。
(提出问题)实验A中蜡烛熄灭的原因是什么?
(猜想与假设)
猜想1:烧杯内的氧气被耗尽,所以蜡烛熄灭。
猜想2:烧杯内的二氧化碳含量升高,所以蜡烛熄灭。
(进行实验)
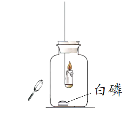
实验I:点燃蜡烛,塞紧胶塞。待蜡烛熄灭后,用放大镜照射白磷。观察到白磷燃烧。
实验II:经检测,实验A中,蜡烛熄灭时,烧杯内二氧化碳的体积分数约为3%。在集气瓶中按照一定的体积比收集气体,分别放入燃烧的蜡烛和燃烧的红磷,实验记录如下:
V(O2):V(CO2) | 蜡烛 | 红磷 |
1:4 | 燃烧 | 燃烧 |
1:5 | 燃烧 | 燃烧 |
1:6 | 熄灭 | 燃烧 |
1:9 | 熄灭 | 燃烧 |
(解释与结论)
(1)实验B中蜡烛熄灭,体现二氧化碳的化学性质是_______。
(2)实验I的目的是_______。
(3)写出红磷燃烧的化学方程式_______。
(4)实验II证明猜想2错误,依据的实验现象是_______。
(5)结合实验I与实验II,得出的实验结论是_______。
(实验反思)
(6)通过此实验,同学们对物质燃烧的条件有了新的认识,如_______。