题目内容
【题目】化学用语是学习化学的基本工具,请用化学符合或化学式填空:
(1)2个铁原子________;
(2)氦气_________;
(3)5个一氧化碳分子___________;
(4)2个铵根离子________;
(5)最清洁的气体燃料__________;
(6)3个亚铁离子______________
(7)标出五氧化二磷中磷的化合价_________;
【答案】2Fe He ![]()
![]() H2 3Fe2+
H2 3Fe2+ ![]()
【解析】
本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其他位置加上合适的数字来完整的表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
(1)原子的表示方法是用元素符号来表示一个原子的,表示多个原子时,就在其元素符号前加上相应的数字,故2个铁原子可表示为2Fe。
(2)氦气属于稀有气体单质,直接用元素符号表示其化学式,其化学式为He。
(3)分子的表示方法是正确书写物质的化学式,表示多个分子时,就在其化学式前加上相应的数字,故5个一氧化碳分子可表示为![]() 。
。
(4)离子的表示方法是在表示该离子的元素符号右上角标出该离子所带的正负电荷数,数字在前,正负号在后, 带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故2个铵根离子可表示为![]() 。
。
(5)氢气燃烧的产物只有水,故H2是最清洁的气体燃料。
(6)根据(4)中表述离子的表示方法,3个亚铁离子可表示为3Fe2+。
(7)化合价的表示方法是在该元素的正上方用正负号和数字表示,正负号在前,数字在后,故标出五氧化二磷中磷元素的化合价可表示为![]() 。
。

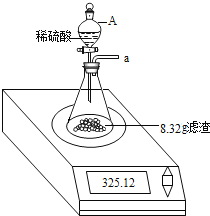
【题目】科学探究是学习化学重要而有效的学习方法。某校化学兴趣小组的同学以酸为专题,对酸的五种化学性质进行探究、总结及应用,请回答有关问题:
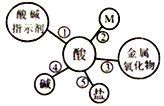
(1)酸的化学性质①一一酸与酸碱指示剂的作用。酸能使紫色石蕊溶液变成红色,不能使无色酚酞溶液变色。
(2)酸的化学性质②,图中M所代表的物质类别是_______。黄金是一种常见饰品,现实生活中,少数商贩用黄铜冒充黄金出售,可以用化学的方法加以鉴别。某同学为了测定黄铜(铜锌合金)样品的成分,将60g稀HCl分三次加入到盛有10g该样品的烧杯中,所得数据如下表,则该黄铜样品中含锌的质量分数为___________。
实验次数 物质质量 | 第1次 | 第2次 | 第3次 |
加入稀盐酸质量/ g | 20 | 20 | 20 |
充分反应后剩余固体质量/g | 8.7 | 7.4 | 6.4 |
(3)酸的化学性质③一一酸与金属氧化物的反应。盐酸可用于金属制品表面除锈等。
(4)酸的化学性质④一一酸碱中和反应。
该校化学兴趣小组的同学重点以“酸碱中和反应”为课题进行探究。小宇同学向烧杯中的氢氧化钠溶液中滴加稀硫酸,一会儿后发现忘了滴加酸碱指示剂,于是他停止滴加稀硫酸。同学们纷纷对实验烧杯溶液中含有哪些溶质展开了讨论。
[提出问题]实验的烧杯中溶质含有哪些物质?
[提出猜想]猜想一 :溶质中只有Na2SO4
猜想二:溶质中可能是Na2SO4和NaOH
猜想三:溶质中可能是____________________。
[查阅资料] Na2SO4溶液呈中性
[实验探究]小宇同学设计如下的实验方案
方法步骤 | 实验现象 | 实验结论 | |
方案一 | 取少量烧杯中的溶液于洁净的试管中, 滴入几滴无色酚酞溶液 | 酚酞不变红色 | 猜想一正确 猜想二不正确 |
方案二 | 取少量烧杯中的溶液于洁净的试管中, 滴加BaCl2溶液 | 出现白色沉淀 | 猜想三正确 |
方案三 | 取少量烧杯中的溶液于洁净的试管中,入少量的黑色CuO粉末,振荡 | _________ | 猜想三正确 |
[方案评价]同学们对小宇上述的方案讨论后认为:
①方案一存在缺陷,该方案不能证明猜想一是正确的,其原因是____________________。
②方案二也不能证明猜想三是正确的,理由是__________________________________。
③同学们经过讨论,一致认为方案三能够证明猜想三是正确的,并讨论除此方案外,还可以向烧杯的溶液中加入活泼金属、碳酸盐等物质进行证明。
[实验反思]在分析化学反应后所得物质成分时,还需考虑反应物的用量。
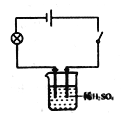
[学科渗透]如图所示,小宇同学在进行溶液导电性的实验时,将电极两端插入稀H2SO4溶液中,闭合开关,小灯泡正常发光,然后逐滴向稀H2SO4中加入Ba(OH)2溶液至过量,请推测小灯泡的发光情况为__________________;发生反应的化学方程式是___________。
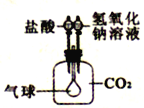
(5)酸的化学性质⑤一一酸与盐的反应
利用下图所示装置来验证CO2气体的性质,要证明CO2与NaOH溶液能够发生反应,可先加氢氧化钠溶液,再加盐酸,气球的变化是_____________。
[方法感悟]在化学实验中,可通过验证反应后生成物的存在,来验证某化学反应的发生。