��Ŀ����
����Ŀ��������ڲ�ͬ�¶��µ��ܽ���������±���ʾ��
�¶�/�� | 0 | 20 | 40 | 60 | 80 |
�ܽ�ȣ�g/100gˮ�� | 13.3 | 31.6 | 63.9 | 110 | 169 |
�ش��������⣺
������ص��ܽ�����¶����߶�___�������С������
��20��ʱ����15������ؼ���40��ˮ�У���ֽ��裬������ҺΪ____������͡������͡�����Һ����ʱ��Һ��������������Ϊ______���г�����ʽ����
��ij����ع����л��������Ȼ��ƣ������ᴿ����صIJ�������ɸ����µ�����ر�����Һ��_______�����ˡ�ϴ�ӡ����
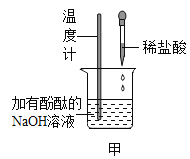
�ܼ���60����������Һ������ͼ��ʾ���в�����������ȷ����____������ţ���
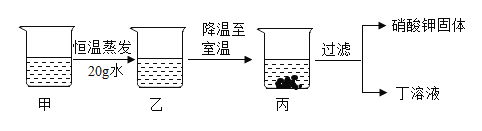
A ��һ���Dz�������Һ
B ���Ͷ�һ���DZ�����Һ
C �ҵ���������������һ���ȼ״�
D �ͱ����������������п������
���𰸡����� ���� ![]() ����
����![]() �� ���½ᾧ B D����©�����֣�
�� ���½ᾧ B D����©�����֣�
��������
���ɱ��������ݿ�֪������ص��ܽ�����¶����߶�����
��20��ʱ������ص��ܽ��Ϊ31.6g����15������ؼ���40��ˮ�У���ֽ��裬ֻ���ܽ�12.64g����أ�������ҺΪ������Һ��![]() ����ʱ��Һ��������������Ϊ
����ʱ��Һ��������������Ϊ![]() ��
��![]() ��
��
������ص��ܽ�����¶�Ӱ��ϴ������¶����߶������Ȼ��Ƶ��ܽ�����¶�Ӱ���С��ij����ع����л��������Ȼ��ƣ������ᴿ����صIJ�������ɸ����µ�����ر�����Һ�����½ᾧ�����ˡ�ϴ�ӡ����
��A������Һ�ں���������20gˮû����������������Լ���Һһ���Dz�������Һ���ҿ����DZ�����Һ��Ҳ�����Dz�������Һ����A����
B������Һ�ײ���δ�ܽ�Ĺ��壬�����DZ�����Һ���Ӷ���Һ����˳�������ع��壬����ҺҲ�DZ�����Һ����B��ȷ��
C��������Һ��ܼ��������ȼ���Һ���ܼ�������20g�������ҵ�������������һ���ȼ״�C����
D����֪������Һ���������پ��壬����Һ������Һ��Ũ�����Ƚϣ�������ȣ�Ҳ���ܲ��ȣ���D��ȷ��
��ѡBD��

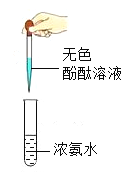
����Ŀ�����̰���꼶��ѧ�²�P197�����б��������ڽ������˳���У�λ����ǰ��Ľ��������ᷴӦ�û�����������
��������⣩С��ͬѧ���Ķ��α�ʱ������⣬ϡ�����Ũ���ᷴӦ�Ƿ���ͬ��λ����ǰ��Ľ������û�Ũ�����е�������������ͬѧ��һ�������ʵ��̽����
��ʵ��̽��1��С��ͬѧ���������ʵ�鷽��������¼��ʵ������
ʵ�� | ����ҩƷ | Һ��ҩƷ | ���� |
�� | ��Ƭ5g | 5%������25mL | ����ɫ��ζ�������������Ӧ�ٶȽ��� |
�� | ��Ƭ5g | 37%������25mL | ����ɫ��ζ�������������Ӧ�ٶȺܿ� |
��1��д��ʵ����з�Ӧ���ɵ��εĻ�ѧʽ��_____��
��2������ʵ����Ƶ�˼�뷽����_____��
��3������֤ʵ��ٺ͢ڲ����������ΪH2���ɴ�С��ͬѧ�ó�λ����ǰ��Ľ������û���ϡ�����Ũ�����е��⣻������ʵ�黹�ܵó��Ľ�����_____��

��ʵ��̽��2�����ұ�����λͬѧ�ֱ����������ĸ�ʵ�飬�۲��������жԱȡ�
��1����ͬѧ�۲������ݲ�����д����Ӧ�Ļ�ѧ����ʽ_____��
��2����ͬѧ��ʵ������˵����Ũ�ȵĸı�Ҳ��Ӱ�����ʵ�_____��������ѧ�����������������ʡ�
��3����ͬѧʵ��ʱ���ֲ������ݵ��ٶȱȼ�ͬѧ�죬˵������_____��ʹ��Ӧ�ӿ졣
��4����ͬѧʵ��ʱ�ŵ��д̼�����ζ������������������Ϻ�ʵ����֤��֪�������ǵ����������Ҫ���ʣ����������_____��д��ѧʽ������ʵ��˵����п��Ũ�����ڼ���ʱ�ܷ�����Ӧ����Ӧ����_____�����������������������û���Ӧ��
�����۷�˼����̽����Ļ�ѧ����ʱ���̲��е�ԭ��ǿ��ϡ�����ԭ����_____��
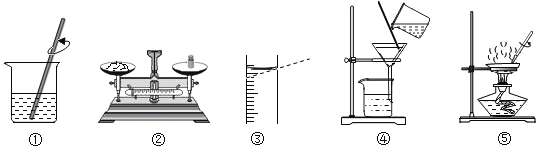
����Ŀ������ʵ����������ȷ����
ѡ�� | A | B | C | D |
ʵ�� |
|
|
|
|
ʵ������ | ����ȼ�գ��������䣬�ų��������ȣ����ɺ�ɫ���� | ���ְ�ɫ���� | ��Һ����ɫ��Ϊ��ɫ | �������ݣ���Һ��Ϊdz��ɫ |
A.AB.BC.CD.D