题目内容
【题目】大理石广泛存在于自然界,某种大理石除主要成分为CaCO3 外,还有少量的硫化钙。甲和乙两位同学用这种大理石和稀盐酸反应,分别开展以下探究,请你参与探究并回答相关问题。
[资料一]:常温下,测得浓度均为a%的下列六种溶液的pH大小:H2SO4<HCl<H2S<H2CO3<HClO
复分解反应的其中一条规律为:较强酸发生类似反应可以生成较弱酸。
(1)下列反应均能发生,其中不符合上述规律的是____________(填字母)
A ![]()
B ![]()
C ![]()
D ![]()
[资料二]:常见干燥剂有①浓硫酸 ②无水氯化钙 ③碱石灰 ④生石灰
[实验探究] 甲同学为了得到纯净的二氧化碳,设计了如下装置,请

(2)制备的CO2气体中,可能含有的杂质是_________ ;
(3)上述装置中,A 是______溶液,NaHCO3溶液可以吸收 ____;
(4)上述装置中,B 物质的名称可能是_________;
(5)将制得的纯净的二氧化碳气体通入氯化钡溶液中,根据资料一判断,____(填“有” 或“没有”)化学反应发生。
【答案】D HCl、H2S、H2O CuSO4 HCl 气体 无水氯化钙 没有
【解析】
(1)根据较强酸发生类似反应可以生成较弱酸进行判断
A、反应物是硫酸,生成物是碳酸,硫酸酸性大于碳酸,符合规律;
B、反应物是盐酸,生成物是氢硫酸,盐酸酸性大于氢硫酸,符合规律;
C、反应物是碳酸,生成物是次氯酸,碳酸酸性大于次氯酸,符合规律;
D、反应物是氢硫酸,生成物是硫酸,氢硫酸酸性小于硫酸,不符合规律;故选D;
(2)若用这种大理石和稀盐酸制备的CO2,硫化钙会和盐酸反应生成H2S,所以可能含有的杂质是HCl、H2S、H2O;
(3)利用上述装置净化二氧化碳,首先将气体通入硫酸铜溶液,除去H2S,再通入碳酸氢钠溶液,除去HCl,最后经无水氯化钙干燥,即可得到纯净的CO2;所以A是CuSO4溶液,NaHCO3溶液可以吸收HCl;
(4)上述装置中,B物质是无水氯化钙,因为B为固体,而碱石灰能和二氧化碳反应,生石灰能和二氧化碳、水反应;
(5)将制得的纯净的二氧化碳气体通入氯化钡溶液中,没有化学反应。如果加入有化学反应,二氧化碳和氯化钡反应生成碳酸钡和盐酸,碳酸的酸性小于盐酸,不符合较强酸发生类似反应可以生成较弱酸,故反应不能发生。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案【题目】阅读下面科普短文。
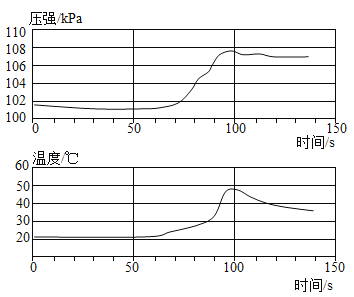
炭烧酸奶近年来发展迅速,其焦香浓郁的风味深受消费者喜爱。炭烧酸奶在制作过程中通过牛奶的长时间褐变,获得浓郁的焦香风味。牛奶褐变,是一系列化合物受热发生反应的过程。褐变生产工艺中需对葡萄糖用量、褐变温度和褐变时间三个重要条件进行严格控制。葡萄糖用量与产品颜色、风味密切相关,具体影响如图 2 所示,其中评分越高,产品的颜色、风味越好。褐变温度和时间的组合是调节蛋白稳定、避免沉淀分层的重要因素,具体影响如表所示,其中沉淀率越低产品越稳定。



表:褐变温度和时间对牛奶褐变沉淀率的影响
褐变温度/℃ | 86 | 88 | 90 | 92 | 94 | 96 |
褐变时间/h | 6 | 4 | 3.5 | 3 | 2.5 | 2 |
沉淀率/% | 0.35 | 0.31 | 0.27 | 0.22 | 0.14 | 0.44 |
优质的制作工艺可使炭烧酸奶口感爽滑,在保质期内状态稳定。依据文章内容回答下列问题。
(1)葡萄糖(C6H12O6)的相对分子质量是180,计算式为______。
(2)制作炭烧酸奶的原料有___________。
(3)牛奶褐变过程中,影响蛋白稳定的因素有_____________。
(4)由图表可知,牛奶褐变过程的最佳条件为_________。
(5)下列说法正确的是______(填序号)。
A 炭烧酸奶的特色是其浓郁的焦香风味
B 葡萄糖用量影响产品的颜色和风味
C 褐变温度越高,炭烧酸奶产品越稳定
D 炭烧酸奶制作过程中需将各种原料一次性混合均匀
【题目】化学课堂上要学习碱的化学性质,老师让两位同学和他共同做实验,要求两位同学分别向澄清石灰水和氢氧化钠溶液中吹气,如图①②所示,老师告诉同学们,呼出的气体中只有二氧化碳有可能与澄清石灰水和氢氧化钠溶液反应。
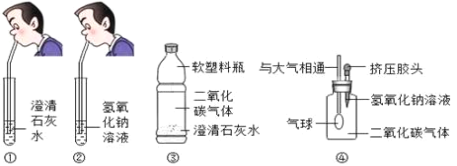
同学们在吹气后观察到①中澄清石灰水变浑浊,②中氢氧化钠溶液无明显现象。观察实验现象后老师问,通过实验现象的观察,检验二氧化碳气体应该使用________,针对②中的情况,师生共同开始探究之旅。
(提出问题)二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
(猜想假设)猜想A:两者发生了化学反应;猜想B:两者没有发生化学反应。
(实验探究)
Ⅰ:小明设计了如图所示的③、④两个实验。
实验现象:③中的软塑料瓶________________,④中气球膨胀。
II:小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低,小光同学却对此提出了质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是___________。
III:小光设计的是通过检验生成物来验证猜想,请帮他填写实验报告:
实验步骤 | 实验现象 | 实验结论 |
取④实验后的溶液少许,再向其中加入____________。 | _________ | 验证了二氧化碳和氢氧化钠溶液反应。 |
(实验结论)二氧化碳和氢氧化钠溶液发生了化学反应。
(反思拓展)实验②中反应后所得溶液中溶质成分:猜想(1):只有碳酸钠;猜想(2):__________。
(数据处理)
小明将实验③中浑浊的液体进行_______(填操作名称)、洗涤、烘干,称量所得固体质量为1.0g。试计算:实验③中参加反应的二氧化碳的质量为____________克?(列式计算)