题目内容
【题目】下列有关实验现象的描述正确的是(____)
A硫在空气中燃烧,发出明亮的蓝紫色火焰
B铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
C氢气在空气中燃饶,产生淡蓝色火焰,放出大量的热
D镁在在空气中燃烧,发出______
【答案】C 耀眼的白光
【解析】
A、硫在空气中燃烧发出淡蓝色火焰,故A不正确;
B、铁丝在空气中不能燃烧,有红热现象,故B不正确;
C、氢气在空气中燃饶,产生淡蓝色火焰,放出大量的热,故C正确。故选C。
D、镁条在空气中燃烧发出耀眼的白光。

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
【题目】以电石渣[主要成分Ca(OH)2和CaCO3]为原料制备KClO3的流程如图。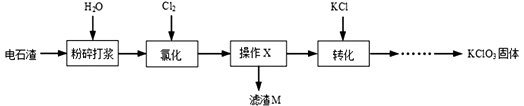
查阅资料:在75℃左右,氯化步骤中氯气转化成Ca(ClO3)2时发生一系列的反应,其中Cl2与Ca(OH)2反应的总化学方程式可表示为:
6 Ca(OH)2 + 6 Cl2 = Ca(ClO3)2 + 5CaCl2 + aH2O
(1)氯化前,先将电石渣粉碎的目的是。
(2)氯化步骤中所得产物氯酸钙Ca(ClO3)2中Cl的化合价为价,a数值为
(3)操作X为。转化步骤中Ca(ClO3)2与KCl反应生成KClO3的化学方程式为。(相关物质的溶解度见下图)
物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
T℃时溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(4)对滤渣M的成分进行探究
【提出问题】滤渣M中除了电石渣原有的不溶性杂质外,还含有什么物质?
【猜想假设】①CaCO3; ②Ca(OH)2; ③。
【实验验证】
实验步骤 | 实验现象 | 结论 |
步骤1:取少量滤渣M加入盛水的小烧杯中,搅拌,静置后先加入; | 观察到现象 | 猜想①不正确 |
步骤2:向小烧杯中继续加入足量的稀盐酸 | 观察到现象 | 猜想③正确 |