题目内容
【题目】水是最普通、最常见的物质之一。
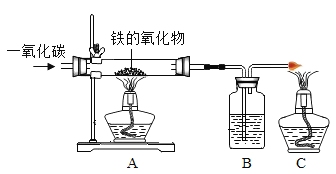
某学校兴趣小组的同学,取学校附近民心河的水样,利用图(1)所示的实验过程对该水样进行了净化处理。请回答下列问题:
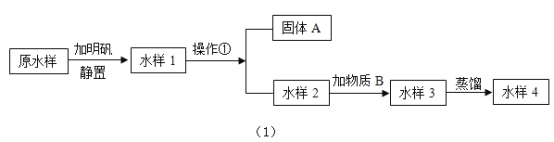

(1)明矾的作用是_________。
(2)为除去水样2中的一些异味和色素,加入的物质B是______。
(3)取少量水样3于试管中,加入少量__________,振荡,发现有较多浮渣产生,说明水样3是________水(填“软”“硬”)。
(4)根据净化过程,判断水样1、水样2、水样3和水样4中净化程度最高的是________。
(5)用于自来水的消毒剂除氯气以外,还可用次氯酸钠( NaClO)、二氧化氯等物质。
①二氧化氯的化学式为___________。
②NaClO中钠、氯、氧三种元素的质量比是________________(结果以最简整数比表示)。
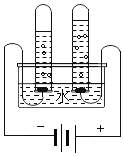
(6)在化学变化中常常伴有能量的变化,通常表现为吸热或放热的现象,某同学用如图(2)所示装置进行过氧化氢分解的实验,反应的化学方程式为:_____________,实验过程中观察到烧杯内导管口有气泡冒出,产生此观象的原因是________________。
【答案】吸附悬浮在水中的固体杂质,使之沉降 活性炭 肥皂水 硬 水样4 ClO2 46:71:32  过氧化氢在二氧化锰催化作用下反应放热,使吸滤瓶中的空气受热膨胀
过氧化氢在二氧化锰催化作用下反应放热,使吸滤瓶中的空气受热膨胀
【解析】
(1)为了使悬浮在水中的固体杂质沉降下来,加入明矾形成胶体,可以吸附这些悬浮的固体杂质使之沉降。故填:吸附悬浮在水中的固体杂质,使之沉降。
(2)活性炭可以除去溶解在水中的颜色和异味,所以为除去水样2中的一些异味和色素,加人的物质B是活性炭。故填:活性炭。
(3)鉴别硬水和软水用的是肥皂水,向水样中加入肥皂水,振荡,如果出现泡沫多、浮渣少现象,水样就是软水,如果出现泡沫少、浮渣多的现象就是硬水。该水样有较多浮渣产生,说明水样3是硬水。故填:肥皂水;硬。
(4)根据净化过程,水样1是沉淀,是固体沉入水样底部后得到的,水样2 是过滤,是除去固体不溶物后得到的,水样3是吸附,是除去溶解在水中的颜色异味后得到的,水样4是蒸馏后得到的,蒸馏得到的水是纯水,所以水样4的净化程度最高。故填:水样4。
(5)①根据化学式的读法(从右向左读)二氧化氯的化学式为ClO2。故填:ClO2。
②NaClO中钠、氯、氧三种元素的质量比是23:35.5:16,以最简整数比表示46:71:32。故填:46:71:32。
(6)过氧化氢在二氧化锰作催化剂的条件下分解产生水和氧气,反应的化学方程式为: ,因为该实验过程放热,使得吸滤瓶中的气体受热膨胀,所以观察到烧杯内导管口有气泡冒出。故填:
,因为该实验过程放热,使得吸滤瓶中的气体受热膨胀,所以观察到烧杯内导管口有气泡冒出。故填: ;过氧化氢在二氧化锰催化作用下反应放热,使吸滤瓶中的空气受热膨胀。
;过氧化氢在二氧化锰催化作用下反应放热,使吸滤瓶中的空气受热膨胀。

【题目】某兴趣小组在实验室中探究氢氧化钾的性质,请你参与他们的探究。
(1)[实验过程与分析]
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
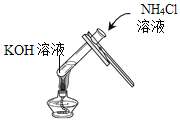
实验现象 | _____________________ | ______________________ | 无明显现象 |
实验结论 | 氢氧化钾能与硫酸铜发生反应 | 氢氧化钾能与氯化铵发生反应 | 氢氧化钾不能与硫酸发生反应 |
实验一反应的化学方程式为_______________。
(2)[实验反思与拓展]
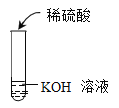
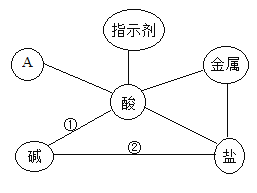
①某同学认为实验三的结论错误。他取适量的氢氧化钾溶液于一支干净的试管中,滴加几滴_________________,溶液呈红色,然后逐滴滴加稀硫酸,直至溶液变成___________色,证明氢氧化钾能与硫酸发生反应。
②对于无明显现象的化学反应,可通过检验有新物质生成或检验_________________的方法来证明物质间发生了化学反应。
【题目】请从A~D中任选三个作答,若均作答,按前三个计分。
实验目的 | 实验 | 回答问题 |
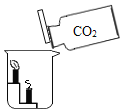
A 验证二氧化碳的密度比空气大 |
| 该实验除了验证CO2的密度比空气大之外,还能说明CO2 具有__________性质。 |
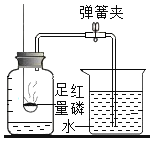
B 探究空气 中氧气含量 |
| 红磷燃烧的作用是 ______。 |
C 证明水的组成 |
| 该 反应的化学方程式 _____ |
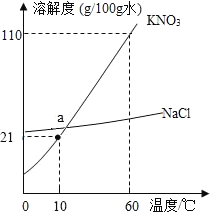
D 检验NaCl中混有Na2CO3 |
| ①加入少量样品;②加入适量水至全部溶解;③加入____有气泡产生。 |