题目内容
【题目】现有A、B、C、D、E五种物质,其中含有Fe 、AgNO3、Cu(NO3)2和一种未知的无色溶液(含一种溶质)和红棕色粉末。且它们有如下反应和转化关系(连线表示两种物质能反应;箭号表示两种物质相互转化)。试回答问题:

(1)写出下列物质化学式:C_______;D________
(2)B和C反应的现象是________________;
(3)写出一个由E→B的化学反应方程式_______________;
(4)将Fe 、AgNO3、Cu(NO3)2放到在一个烧杯中,充分反应后过滤,向滤液中滴加稀盐酸,无任何现象,则滤渣中可能含有的金属是_____________。
【答案】Cu(NO3)2:HCl C:O2; 银白色物质表面有(紫)红色物质析出,溶液由蓝色变为(浅)绿色; 3CO+Fe2O3![]() 2Fe +3CO2 Cu
2Fe +3CO2 Cu
【解析】
红棕色粉末是氧化铁;Fe2O3粉末能与盐酸生成反应氯化铁和水,稀盐酸能与铁反应生成氢气和氯化亚铁,盐酸和硝酸银反应能生成氯化银和硝酸,铁和硝酸铜反应生成铜和硝酸亚铁,且氧化铁和铁之间可相互转化,铁生锈可生成氧化铁,氧化铁和一氧化碳高温下可生成铁和二氧化碳,综上述分析可知:A是硝酸银,B是铁单质,C是硝酸铜,D是盐酸,E是氧化铁。
由分析可知(1)C的化学式为Cu(NO3)2;D的化学式为HCl;
(2)B为铁单质,C是硝酸铜,两者反应可生成铜和硝酸亚铁,反应的现象为银白色物质表面有(紫)红色物质析出,溶液由蓝色变为(浅)绿色;
(3)氧化铁和一氧化碳在高温下可生成铁和二氧化碳,反应的化学方程式为3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(4)铁在银和铜的前面,因此铁可以和硝酸银、硝酸铜反应,滤液中加入稀盐酸,无任何现象,说明滤液中不会有AgNO3(硝酸银能与盐酸反应生成白色的氯化银沉淀),所以滤渣中一定会含有银,滴加稀盐酸,无任何现象,一定没有铁,则可能含有铜。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】碘化钾(KI)保存不当会变质。实验小组进行以下实验探究KI变质的因素。
(提出问题1) KI变质的条件是什么?
(查阅资料)
① KI为白色粉末,暴露在空气中或久置会被氧化为碘(I2)而泛黄变质。
② 碘水中含较多KI时,滴加淀粉溶液显紫色或蓝紫色
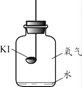
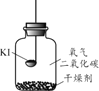
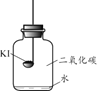
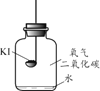
(进行实验)分别取适量KI于燃烧匙中,再分别放入盛有不同物质的集气瓶中,塞紧胶塞,若干天后观察。
实验1 | 实验2 | 实验3 | 实验4 |
|
|
|
|
固体变潮、表面变微黄 | 固体无明显现象 | 固体变潮、无其他明显现象 | 固体变潮、表面变黄 |
继续实验:取实验1中少量微黄固体溶解,加入淀粉溶液,溶液变紫色。
取实验4中少量黄色固体溶解,加入淀粉溶液,溶液变紫色。
(解释与结论)
(1)实验3的目的是_______。
(2)对比实验_______,可以得出KI变质一定与水有关。
(3)从上述实验可推知,KI变质的条件是_______。
(4)CO2的作用是______。