题目内容
【题目】往 64.5 克稀盐酸和氯化镁的混合溶液中,加入 20%的氢氧化钠溶液,所得溶液的 pH 变化与加入氢氧化钠溶液 的质量关系如图所示,试分析计算:
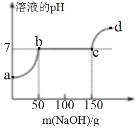
(1)a→b 段表示氢氧化钠与混合溶液中的_______________反应。
(2)反应到 c 点时,所得溶液的溶质质量分数是____________?(精确到 0.1%)
【答案】稀盐酸 21.9%
【解析】
解:根据图可以看出,a→b段是pH变大的阶段,所以是消耗酸的过程,所以为氢氧化钠和稀盐酸的反应;设生成的氯化钠的质量为x,根据钠元素守恒可得关系式为:
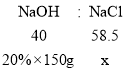
![]()
x=43.875g;
设生成的沉淀氢氧化镁的质量为y,和氯化镁反应的氢氧化钠溶液的质量为150g-50g=100g;
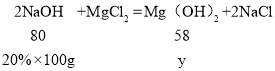
![]()
y=14.5g;
反应到c点时,所得溶液的溶质质量分数为![]() ×100%≈21.9%;
×100%≈21.9%;
答:(1)a→b段表示氢氧化钠与混合溶液中的稀盐酸反应;
(2)反应到c点时,所得溶液的溶质质量分数是21.9%。

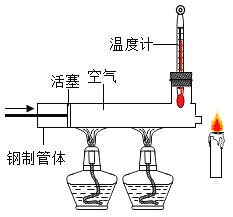
【题目】某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验.
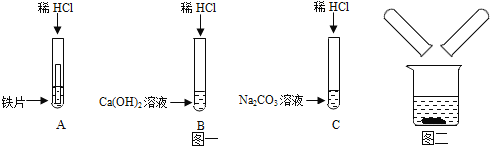
(1)写出A试管中的反应现象_____.
(2)写出B试管中反应的化学方程式_____.
(3)实验结束后,小组同学将_____两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
(提出猜想)
甲同学猜想:NaCl; 乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl; 你的猜想:_____.
(交流讨论)
你认为_____同学的猜想一定不正确,理由是_____.
(设计实验)请设计实验证明你的猜想正确.
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加_____ | _____ | 猜想成立 |
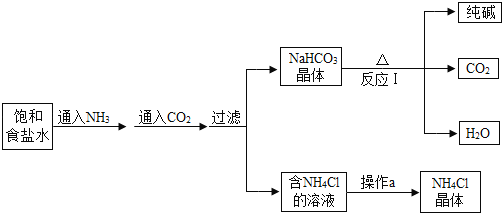
【题目】金属在生产和生活中应用广泛。请回答下列问题。
(1)生活中常用铁锅做饭,主要利用了铁的_____性。
(2)厨房中铁锅容易生锈,结合生活实际,写出一种防止铁锅生锈的具体方法_____。
(3)铝合金制造的飞机外壳,具有轻量化、能抗击强大气流的冲击、耐受水雾和雨雪侵蚀等特点。这是利用了铝合金的_____、_____等优点(写出两条即可)。
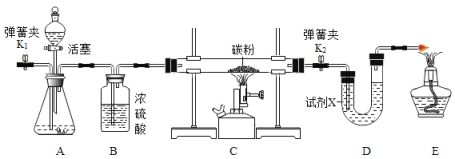
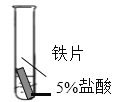
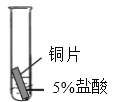
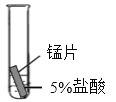
(4)某研究小组为探究铁、铜、锰(Mn)的金属活动性顺序,进行了如下三个实验(其中金属均已打磨,且形状、大小相同,试管中所用 5%的盐酸体积相同)。
(实验记录与分析)
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
实验现象 | 立即产生气泡,速率较慢 | 无明显现象 | 立即产生气泡,速率较快 |
实验结论 | 铁、铜、锰的金属活动性顺序由强到弱为______>______>_____ | ||
写出实验一试管中铁和盐酸发生反应的化学方程式_________________________________________________________________。