题目内容
【题目】向一定质量的AgNO3和Fe(NO3)2的混合溶液中加入a克Zn粉,充分反应后过滤,将洗涤、干燥后称量,得到的固体质量为a克。据此,下列说法正确的是( )
A. 滤液中的物质一定至少有两种
B. 取反应后的滤液滴加稀盐酸,可能有白色沉淀产生
C. 取滤渣滴加稀盐酸,一定有气泡产生
D. 取反应后的滤液观察,滤液一定呈无色
【答案】C
【解析】
在金属活动性顺序中,Zn>Fe>Ag,向一定质量AgNO3和Fe(NO3)2的混合溶液中加入Zn,Zn先AgNO3反应,再与Fe(NO3)2反应;![]() 所以析出银的过程是固体质量增加的过程;
所以析出银的过程是固体质量增加的过程;![]() 所以析出铁的过程是固体质量减少的过程;而反应前后固体质量都是ag,说明硝酸银被置换完了,硝酸亚铁也发生了置换反应,因此滤渣一定含有银和铁,可能含有锌;滤液一定含有硝酸锌,可能含有硝酸亚铁,一定没有硝酸银。
所以析出铁的过程是固体质量减少的过程;而反应前后固体质量都是ag,说明硝酸银被置换完了,硝酸亚铁也发生了置换反应,因此滤渣一定含有银和铁,可能含有锌;滤液一定含有硝酸锌,可能含有硝酸亚铁,一定没有硝酸银。
A、滤液一定含有硝酸锌,可能含有硝酸亚铁,一定没有硝酸银,故A错误;
B、取反应后的滤液滴加稀盐酸,没有沉淀产生,因为硝酸银完全被置换,故B错误;
C、因为滤渣中肯定含有铁,因此取滤渣滴加稀盐酸,肯定有气泡,故C正确;
D、滤液可能含有硝酸亚铁,因此滤液可能呈现浅绿色,故D错误。故选C。

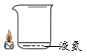
【题目】同学们发现有一种“氮气灭火装置”能利用液氮(沸点为-196℃)产生的大量氮气来灭火。他们用氮气进行如右图所示实验,却发现蜡烛未熄灭。
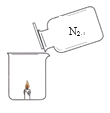
(查阅资料)氮气密度略小于空气;压强不变时,气体温度越低,密度越大。
(1)结合氮气性质分析,右图蜡烛未熄灭的原因可能是_______。
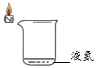
实验1:探究氮气能否用来灭火(所用容器均为隔热材料,下同)
实验编号 | 1-1 | 1-2 | 1-3 |
实验内容 |
|
|
|
实验现象 | 蜡烛持续燃烧 | 蜡烛缓慢熄灭 | 蜡烛熄灭 |
(2)实验前有同学提出,由液氮汽化产生的氮气温度低,密度足够大,会向下流动隔 绝可燃物周围的氧气。依据实验1判断,这种假设_____(填“成立”或“不成立”)。
(3)有同学根据实验1提出新假设,氮气灭火可能与可燃物周围氮气的含量有关。可 能支持这一假设的实验现象是_______(填实验1中的实验编号)。
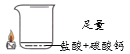
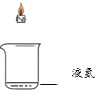
实验2:探究灭火与氮气含量是否有关
实验编号 | 2-1 | 2-2 | 2-3 |
实验内容 |
|
|
|
实验现象 | 蜡烛没有熄灭 | 蜡烛缓慢熄灭 |
(4)实验2中,蜡烛所在位置氮气含量最高的是_________(填实验编号)。
(5)推测实验2-3的现象是________。
(6)反思实验2,除氮气含量外,影响蜡烛燃烧的其它可能因素是________。
(7)结合上述实验,下列关于 “氮气灭火装置”使用的说法中,合理的是______(填字母序号)。
A. 从高处向低处喷洒使用
B. 可燃物火焰熄灭后,还需持续通气一段时间
C. 在有少量排气口的封闭空间中使用时,效果好于开放空间