题目内容
【题目】向100g氢氧化钡溶液中滴加溶质质量分数为10%的硫酸铜溶液,溶液的导电能力随着硫酸铜溶液的加入发生如图的变化关系。
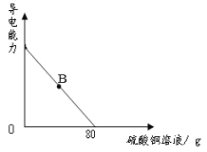
(1)溶液的导电能力逐渐减弱的原因是_____。
(2)溶液处于B点时,其中含有的微粒是OH-和_____(填微粒符号)。
(3)计算氢氧化钡溶液的溶质质量分数。_____
【答案】反应过程中溶液可自由移动离子在不断减少 Ba2+、H2O 8.55%
【解析】
(1)氢氧化钡与硫酸铜反应生成硫酸钡沉淀和氢氧化铜沉淀,溶液的导电能力逐渐减弱的原因是反应过程中溶液可自由移动离子在不断减少;
(2)当溶液处于B点时,氢氧化钡溶液过量,硫酸铜溶液不足,因此溶液中含有的微粒有:OH-、Ba2+、H2O;
(3)根据图示可知,100g氢氧化钡与80g的硫酸铜溶液恰好完全反应,80g的硫酸铜溶液中硫酸铜的质量= 80g×10%=8g。
设:氢氧化钡溶液中的溶质质量为x
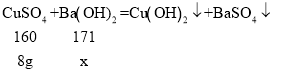
![]() x=8.55g;
x=8.55g;
氢氧化钡溶液的溶质质量分数=![]() 。
。
答:氢氧化钡溶液的溶质质量分数8.55%。

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目