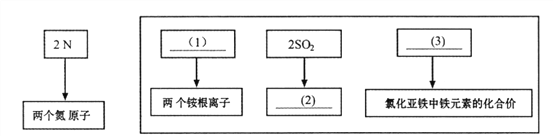
题目内容
【题目】氨催化氧化是制硝酸的主要反应之一。该反应的微观示意图如下,其中 D 是一种常见 的氧化物。
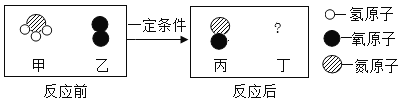
(1)反应前后化合价发生改变的元素是__________________
(2)请在答题卡框内画出 D 的微观结构图像。__________
(3)该反应的化学方程式是__________。
【答案】氧元素和氮元素  5O2+4NH3
5O2+4NH3 4NO+6H2O
4NO+6H2O
【解析】
由微观示意图可列出反应方程式:O2+NH3→NO+D,由质量守恒定律,且D 是一种常见 的氧化物,可知D为H2O。则氨催化氧化的反应方程式为5O2+4NH3=4NO+6H2O。
(1)由反应方程式可知,反应前后化合价发生改变的元素是氧元素和氮元素。
(2)H2O的微观结构图像
(3)由分析可知,氨催化氧化的反应方程式为5O2+4NH3 4NO+6H2O
4NO+6H2O

【题目】2009年邵阳市九年级化学实验操作技能考试中,小聪同学抽到的试题是“探究酸和碱之间的中和反应“。他向盛有氢氧化钠溶液的烧杯中缓慢滴加稀盐酸,一会儿后,想起忘记加指示剂了,便补加几滴无色酚酞溶液,搅拌,观察到溶液不变色,于是他得出“酸碱恰好完全中和”的结论。
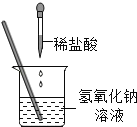
(1)该中和反应的化学方程式是_____;
(2)老师给予小聪的评定是结论不准确。请你帮小聪分析老师的理由是:_____
(3)请你另外设计一个实验,探究小聪实验后烧杯中的溶液是否“恰好完全中和”。
填写下表:
实验步骤 | 实验现象 | 实验结论 |
_____ | _____ | _____ |
_____ | _____ |
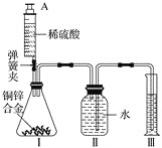
【题目】为了探究金属活动性,将锌和铜分别放入稀硫酸中,铜不反应而锌的表面有气泡产生。老师告诉学生,铜和浓硫酸在加热的条件下也能反应且产生气体。
(提出问题)铜与浓硫酸反应的生成物是什么?其中气体是什么?
(猜想假设)同学们对产生的气体作出了猜想。
猜想一:氢气; 猜想二:二氧化硫;
猜想三:氢气和二氧化硫的混合物。
(查阅资料)(1)二氧化硫可以使品红溶液褪色,也能和碱性溶液反应
(2)H2+CuO![]() Cu+H2O
Cu+H2O
(实验探究)师生设计了如下装置进行实验(部分仪器省略),请完成下列表格。

主要实验步骤 | 主要现象 | 解释或结论 |
①加热装置A一段时间 | 装置B中的品红溶液褪色 | 有_____生成 |
②点燃装置D处酒精灯 | 装置D玻璃管中无明显现象 | 猜想____正确 |
③停止加热,将铜丝上提,向装置A中玻璃管鼓入空气 | / | / |
④冷却,将A中液体用水稀释 | A中液体变为____色 | 有硫酸铜生成 |
(表达交流)
(1)在步骤③中,鼓入空气的目的是____________________。
(2)请完成铜与浓硫酸反应的化学方程式:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+_______
CuSO4+SO2↑+_______
(3)若猜想二正确,装置E中发生反应的化学方程式是___________________________。
(反思拓展)
下列各组药品能够证明锌的活动性比铜强的是_____(填序号)。
① 锌、铜、稀盐酸 ② 锌、硫酸铜溶液 ③ 锌、铜、氯化镁溶液
【题目】同学们在学习碱的化学性质时,进行了如图所示的实验。
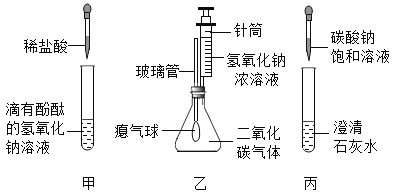
(1)乙实验中滴加氢氧化钠溶液后,可观察到的现象是________。
(2)丙实验中观察到试管内有白色沉淀产生。
实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问。
(提出问题)废液中含有哪些物质?
(交流讨论)①一定含有的物质:碳酸钙、指示剂、水和________(写物质名称)。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有如下猜想。
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是________。(写一种猜想)
(实验设计)小方想用氯化钙溶液来验证小云、小红、小林的猜想。查阅资料获悉氯化钙溶液呈中性,并设计如下实验。请你将小方的实验设计补充完整。
实验内容 | 预计现象 | 预计结论 |
取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置。 | ①有白色沉淀,溶液呈红色。 | ________的猜想正确。 |
②________。 | ________的猜想正确。 | |
③________。 | ________的猜想正确。 |