题目内容
【题目】下列图像能正确反应对应变化的是(____)
A |
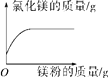
| 向一定质量的盐酸中加入镁粉至过量 |
B |
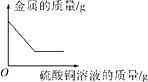
| 向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液 |
C |
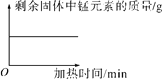
| 加热一定量的高锰酸钾固体 |
D |
| 向氢氧化钠溶液中加入X,X可能是________ |
A. A B. B C. C D. D
【答案】 C 水(或氯化钠溶液等,合理即可)
【解析】A、镁和稀盐酸反应生成氯化镁和氢气,氯化镁的质量从零开始逐渐增加,反应完全后,其质量不在变化,故A错误;B、根据铁和硫酸铜反应的化学方程式:Fe+CuSO4═Cu+FeSO4可以判断消耗的铁的质量要小于生成的铜的质量,所以可以判断反应后金属的质量增加,故B错误;C、高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,剩余固体中锰元素质量不变,故C正确;故选:C。

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案【题目】有一种神奇的蜡烛,任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,那么到底是什么能让蜡烛持续燃烧?请你一起参与探究。
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末,打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃,当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。
【请教老师】老师告诉同学们,蜡烛芯内打火石中的某种金属是镁、铁、铜三种金属中的一种。
【进行实验】为确定该金属的成分,大家设计了以下实验方案。
实验操作步骤 | 实验现象 | 实验结论 |
1.切开蜡烛,取出打火石,用砂纸打磨 | 打火石呈银白色 | 该金属一定不是________ |
2.取少量打磨后的打火石于试管中,滴加稀盐酸 | 有无色气体产生,反应后的溶液呈______色 | 该金属一定不是铁,而是镁 |
【反思交流】(1)实验2中反应的化学方程式为__________________________________。
(2)这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?___________________________;当吹灭蜡烛时,烛芯中的金属燃烧的化学方程式为_________________________________。
(3)这种“吹不灭”的蜡烛实际上也可以熄灭,你采用的方法是______。