题目内容
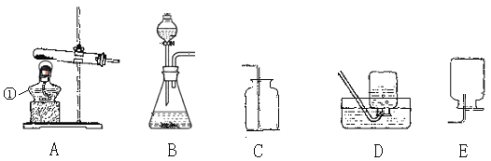
【题目】现有盐酸、氢氧化钠、氢氧化钙三瓶遗失标签的溶液,为了鉴别这些溶液,将它们编号为A、B、C,并按下图步骤进行实验,观察到以下现象:

(1)写出试剂的名称①是 ;②是 .
(2)写出三种溶液的化学式:A 、B 、C .
(3)写出生成白色沉淀的反应的化学方程式 .
(4)写出A与B反应的化学方程式: .
(5)本实验如果将步骤①与步骤②颠倒,能否达到实验目的? .
【答案】(1)①是酚酞,试剂②是碳酸钠;
(2)Ca(OH)2;HCl;NaOH;
(3)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(4)Ca(OH)2+2HCl=CaCl2+2H2O.
(5)能达到目的.
【解析】(1)氢氧化钠和氢氧化钙都是碱,都显碱性,会使酚酞变红色,盐酸显酸性不会使酚酞变色,氢氧化钠和氢氧化钙中阳离子不同,可以加入碳酸钠等,在氢氧化钙中会生成白色沉淀,在氢氧化钠中没有现象,所以加入的试剂①是酚酞,试剂②是碳酸钠;
(2)由题意可知,加入试剂①A、C都显红色,说明A、C具有相同的性质,三种试剂中氢氧化钠和氢氧化钙都是碱,盐酸属于酸,碱会使酚酞变红色,酸不会使酚酞变色,所以加入的试剂①是酚酞;由于氢氧化钠和氢氧化钙中的阳离子不同,所有的钠形成的化合物都溶于水,氢氧化钙会与二氧化碳生成沉淀,故可推断出A为:Ca(OH)2,B为:HCl,C为:NaOH;故答案:Ca(OH)2;HCl;NaOH;
(3)氢氧化钙和试剂碳酸钠溶液发生反应生成白色的碳酸钙沉淀和氢氧化钠;
(4)A和B的反应是氢氧化钙和盐酸反应生成氯化钙和水,其反应化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;
(5)顺序颠倒后可以先利用碳酸钠鉴别出三种物质,遇到碳酸钠产生气体的原溶液是为盐酸,遇到碳酸钠产生沉淀的原溶液是氢氧化钙,无明显变化的原溶液为氢氧化钠;故答案:能达到目的.

【题目】下列图像能正确反应对应变化的是(____)
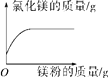
A |
| 向一定质量的盐酸中加入镁粉至过量 |
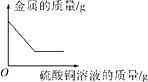
B |
| 向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液 |
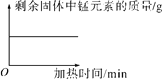
C |
| 加热一定量的高锰酸钾固体 |
D |
| 向氢氧化钠溶液中加入X,X可能是________ |
A. A B. B C. C D. D