题目内容
【题目】浩瀚的大海里蕴藏着丰富的资源,开发海水资源前景广阔,探究学习小组以含有Ca2+、Mg2+、Cl-的卤水和贝壳(主要成分为CaCO3)为主要原料在实验室制备无水CaCl2,流程如图所示:

请回答下列问题:
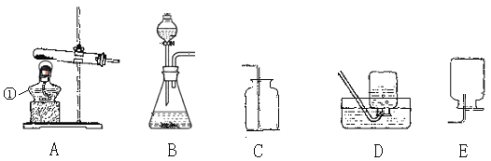
(1)操作Ⅰ中的名称是____,该操作中玻璃棒的作用是______。
(2)以MgCl2为例,写出除去卤水中Mg2+时发生反应的化学方程式:_______。
(3)操作Ⅱ酸化时应选择的酸是____(选填“稀盐酸”或“稀硫酸”)。
(4)海水是天然巨大的“盐库”,我们吃的食盐大都来自海水晒盐,海水晒盐的主要原理是____。
【答案】 过滤 引流 MgCl2+Ca(OH)2===CaCl2+Mg(OH)2↓ 稀盐酸 蒸发结晶
【解析】(1)操作Ⅰ是分离固体与液体的方法,是过滤;在过滤操作中,玻璃棒的作用是引流;(2)由反应的流程可知,除去Mg2+时,加氢氧化钙,氯化镁转化为氢氧化镁的反应是氯化镁与氢氧化钙反应生成了氢氧化镁沉淀和氯化钙,反应的化学方程式是:MgCl2+Ca(OH)2===CaCl2+Mg(OH)2↓;(3)该过程是制取CaCl2,Ⅱ中的酸只能是盐酸;(4)氯化钠的溶解度受温度影响比较小,所以海水晒盐的原理是蒸发结晶。

练习册系列答案
相关题目
【题目】下列图像能正确反应对应变化的是(____)
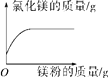
A |
| 向一定质量的盐酸中加入镁粉至过量 |
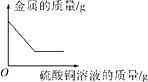
B |
| 向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液 |
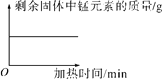
C |
| 加热一定量的高锰酸钾固体 |
D |
| 向氢氧化钠溶液中加入X,X可能是________ |
A. A B. B C. C D. D