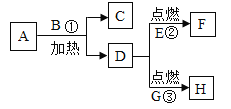
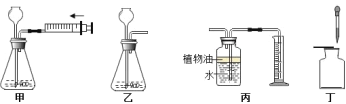
��Ŀ����
����Ŀ������ʹ�õ���ˮ���ײ���һ��ˮ������Ҫ�ɷ���̼��ƣ�CaCO3����ij��ѧ��ȤС��Ϊ�˲ⶨˮ����̼��Ƶ�������������֪25gˮ����ʢ�й�����ϡ������ձ�����100g���ڵ��ӳ��ϻ�Ϻ���������������4������ÿһ���Ӷ�һ������������±����Իش��������⣺
ʱ��/min | 0 | 1 | 2 | 3 | 4 |
����/g | 100g | 95g | 92g | 91.2g | 91.2g |
��1����Ӧ���ɵĶ�����̼�������Ƕ��٣�
��2����ˮ����CaCO3�����������Ƕ��٣�
���𰸡���1����Ӧ���ɵĶ�����̼��������8.8g����2����ˮ����CaCO3����������Ϊ80%��
����������1��̼��ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼���ɱ������ݿ�֪����3��4���Ӻ��ձ��ڵ��������ٱ仯��˵��̼����Ѿ���ȫ��Ӧ����ǰ����ٵ������������ɶ�����̼����������Ӧ���ɵĶ�����̼������Ϊ100g��91.2g=8.8g��
��2�����ˮ����CaCO3��������x��
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 44
x 8.8g
![]()
x=20g
��ˮ����CaCO3����������=![]() =80%
=80%
�𣺣�1����Ӧ���ɵĶ�����̼��������8.8g����2����ˮ����CaCO3����������Ϊ80%��

����Ŀ��ij��ѧѧϰС���ͬѧ��һƿ���ڷ��õ��������ƹ���Ļ�ѧ�ɷֲ�������Ȥ�����Ǹ����Լ���ѧ֪ʶ��������̽����
��������⣩��ƿҩƷ�Ļ�ѧ�ɷ���ʲô��
���������ϣ���1������������������еĶ�����̼��Ӧ�����ʡ�
��2���������Ƶ��ܽ��������ͼ��
�������ܽ������
��������裩����һ��![]() �� �����
�� �����![]() �� ��������_____��
�� ��������_____��
��ʵ����֤��
ʵ����� | ʵ������ | ʵ����� |
��1��ȡlg��Ʒ����ʢ��50gˮ���ձ��У���ֽ������ | �ձ��ײ��н϶����δ�ܽ� | ��Ʒ�к��� |
��2��ȡʵ�飨1�����ϲ���Һ�������Թ��У������Թ��еμ�2��3����ɫ��̪��Һ | _____ | ��Ʒ�к��� |
���ó����ۣ���ͬѧ��Ϊ��������ȷ��
����˼������
��1����ͬѧ��Ϊ��ͬѧ�Ľ��۲�����������Ϊ����_____Ҳ������ȷ��ԭ����_____��
��2����ͬѧ��ΪҪ����֤��������ȷ������������ʵ�飺ȡʵ�飨1����δ�ܽ�������Թ��У����Թ��еμ�����ϡ���ᣬ����_____�����������ȷ��
����չ������
Ҫ����֤��Ӧ�����ʵijɷ֣�������֤�����������⣬��Ӧ���Ƿ�Ӧ���Ƿ�_____��