题目内容
为了从含有硝酸铜的废液中提取金属铜,某化学兴趣小组的同学向废液中加入了一定量锌粉和铁粉的混合物,充分反应后过剩,向滤渣中加入盐酸,有气泡产生.
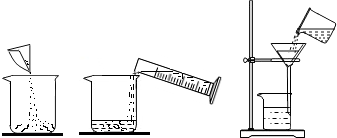
(1)上图所示为实验过程中的相关操作,操作过程中出现的错误是: .
(2)滤液中一定含有的离子是: .(填名称)
(3)加入锌粉和铁粉后,一定发生反应的化学方程式为 .

(1)上图所示为实验过程中的相关操作,操作过程中出现的错误是:
(2)滤液中一定含有的离子是:
(3)加入锌粉和铁粉后,一定发生反应的化学方程式为
考点:金属的化学性质,过滤的原理、方法及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,进行过滤操作时要使用玻璃棒进行引流.据此分析.
解答:解:(1)观察给出的操作题,可以发现进行过滤操作时要使用玻璃棒进行引流,所以本题答案为:过滤时没有用玻璃棒引流;
(2)在金属活动性顺序中,锌>铁>铜,锌能与硝酸铜反应生成硝酸锌和铜,铁能与硝酸铜反应生成硝酸亚铁和铜,锌能与硝酸亚铁反应生成硝酸锌和铁,向滤渣中加入盐酸,有气泡产生,说明滤渣中一定有铁,由于硝酸铜的量不能确定,故铁是否与硝酸铜反应未知,故不能确定溶液中是否含有亚铁离子,所以本题答案为:Zn2+、NO3-;
(3)滤渣中含有铁,锌,锌的活动性比铁强,因此锌一定与硝酸铜反应,铁是否与硝酸铜反应未知,所以本题答案为:Zn+Cu(NO3)2═Zn(NO3)2+Cu.
(2)在金属活动性顺序中,锌>铁>铜,锌能与硝酸铜反应生成硝酸锌和铜,铁能与硝酸铜反应生成硝酸亚铁和铜,锌能与硝酸亚铁反应生成硝酸锌和铁,向滤渣中加入盐酸,有气泡产生,说明滤渣中一定有铁,由于硝酸铜的量不能确定,故铁是否与硝酸铜反应未知,故不能确定溶液中是否含有亚铁离子,所以本题答案为:Zn2+、NO3-;
(3)滤渣中含有铁,锌,锌的活动性比铁强,因此锌一定与硝酸铜反应,铁是否与硝酸铜反应未知,所以本题答案为:Zn+Cu(NO3)2═Zn(NO3)2+Cu.
点评:本题难度较大,主要考查了对金属活动性顺序的应用,从而培养学生的分析能力和应用能力.注意活动性强的金属放入活动性弱的金属的盐溶液中,活动性强的金属会先把活动性最弱的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
向硝酸银和硝酸镁的混合溶液中加入一定量锌粉和铁粉的混合物,充分反应后过滤,得滤渣和滤液,向滤液中加入适量的稀盐酸,无沉淀出现,则下列说法中正确的是( )
| A、滤渣中一定有银、铁,可能有锌,滤液中一定有Mg2+、Zn2+,可能有Fe2+ |
| B、滤渣中一定有银、铁,可能有锌,滤液中一定有Mg2+、Zn2+、Fe2+,可能有Ag+ |
| C、滤渣中一定有银,可能有锌、铁,滤液中一定有Mg2+、Zn2+,可能有Fe2+ |
| D、滤渣中一定有银,可能有锌、铁,滤液中一定有Mg2+、,可能有Zn2+、Fe2+、Ag+ |
 实验室需要质量分数为10%的NaCl溶液,配制质量分数为5%的氯化钠溶液.
实验室需要质量分数为10%的NaCl溶液,配制质量分数为5%的氯化钠溶液. 如图是市售某牙膏的部分说明.其主要成分是单氟磷酸钠(Na2PO3F),它是牙膏的常用添加剂,实验表明,单氟磷酸钠的质量分数达到0.76%--0.80%时,防龋齿效果较好.(②③小题计算结果精确到0.01%)
如图是市售某牙膏的部分说明.其主要成分是单氟磷酸钠(Na2PO3F),它是牙膏的常用添加剂,实验表明,单氟磷酸钠的质量分数达到0.76%--0.80%时,防龋齿效果较好.(②③小题计算结果精确到0.01%)

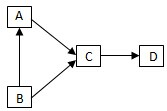 A、B、D都是初中化学常见的氧化物,其中A、B物质的组成元素相同,C为氧气,D是形成酸雨的元凶,它们之间的相互转化关系如图所示(部分反应物、生成物及反应条件已略去).
A、B、D都是初中化学常见的氧化物,其中A、B物质的组成元素相同,C为氧气,D是形成酸雨的元凶,它们之间的相互转化关系如图所示(部分反应物、生成物及反应条件已略去).