题目内容
向硝酸银和硝酸镁的混合溶液中加入一定量锌粉和铁粉的混合物,充分反应后过滤,得滤渣和滤液,向滤液中加入适量的稀盐酸,无沉淀出现,则下列说法中正确的是( )
| A、滤渣中一定有银、铁,可能有锌,滤液中一定有Mg2+、Zn2+,可能有Fe2+ |
| B、滤渣中一定有银、铁,可能有锌,滤液中一定有Mg2+、Zn2+、Fe2+,可能有Ag+ |
| C、滤渣中一定有银,可能有锌、铁,滤液中一定有Mg2+、Zn2+,可能有Fe2+ |
| D、滤渣中一定有银,可能有锌、铁,滤液中一定有Mg2+、,可能有Zn2+、Fe2+、Ag+ |
考点:金属的化学性质
专题:金属与金属材料
分析:在金属活动性顺序中,只有前面的金属可以把排在它后面的金属从盐溶液中置换出来,钾、钙、钠除外;根据金属活动性,判断金属与盐溶液发生反应的关系,并依据滤液中金属离子判断析出金属;根据滤液与稀盐酸反应的现象,判断滤液的组成.
解答:解:由于在这四种金属的活动性顺序为:Mg>Zn>Fe>Ag,因此金属锌和铁都可以和硝酸银溶液反应,但不能和硝酸镁溶液反应,由于锌的活动性比铁强,因此锌首先和硝酸银溶液反应,
向滤液中滴加稀盐酸,无沉淀出现,说明滤液中一定没有硝酸银,由于硝酸银首先和金属锌反应,因此溶液中一定含有锌离子,还有原溶液中的镁离子,可能含有亚铁离子,一定没有银离子,即滤液中一定含有镁离子、锌离子,可能含有亚铁离子,一定没有银离子;滤渣一定含有置换出的银,可能含有铁和锌,一定没有镁;观察选项,故选项为:C.
向滤液中滴加稀盐酸,无沉淀出现,说明滤液中一定没有硝酸银,由于硝酸银首先和金属锌反应,因此溶液中一定含有锌离子,还有原溶液中的镁离子,可能含有亚铁离子,一定没有银离子,即滤液中一定含有镁离子、锌离子,可能含有亚铁离子,一定没有银离子;滤渣一定含有置换出的银,可能含有铁和锌,一定没有镁;观察选项,故选项为:C.
点评:本题难度较大,主要考查了对金属活动性顺序的应用,从而培养学生的分析能力和应用能力.注意金属与盐的混合溶液反应时,置换反应按金属活动性由弱到强的顺序先后反应,首先活动性最强的金属把溶液中活动性最弱的金属从其盐溶液中置换出来.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
下列图示实验操作中,正确的是( )
A、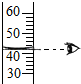 读出液体体积 |
B、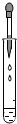 滴加液体 |
C、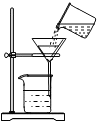 过滤 |
D、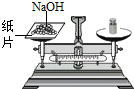 称量氢氧化钠 |
下列做法有利于保护环境的是( )
| A、为清洁城市,将垃圾集中燃烧 |
| B、用煤炭发电 |
| C、将使用后的废旧电池收集起来,统一回收 |
| D、焚烧秸杆 |
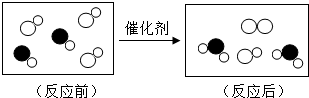 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )| A、此反应有单质生成 |
| B、原子在化学变化中是不可分的 |
| C、参加反应的两种分子的个数比为1:1 |
| D、此反应为置换反应 |
交警常用“司机饮酒检测仪”检查司机是否饮酒.司机呼出气体中的乙醇分子能在硫酸存在的条件下,使红色的三氧化铬变为绿色的硫酸铬[Cr2(SO4)3].关于硫酸铬的说法正确的是( )
| A、硫酸铬中铬、硫、氧三种元素的原子个数比为2:3:12 |
| B、硫酸铬分子中含有两个氧分子 |
| C、硫酸铬中铬的化合价为+2 |
| D、硫酸铬是一种混合物 |
生活中的下列现象,一定发生了化学变化的是( )
| A、酒精挥发 | B、冰雪融化 |
| C、糖溶于水 | D、纸张燃烧 |