题目内容
有一包固体粉末,可能由CaCO3、Na2SO4、KNO3、CuSO4、BaCl2中的一种或几种组成.做实验得以下结果:
①将此固体粉末加到水中,得到白色沉淀,且上层清液呈无色;
②该白色沉淀部分溶于稀硝酸,并有无色气体产生.由以上实验可推断:
(1)这包白色固体中,肯定存在 ; 肯定不存在 ;
(2)写出②中产生无色气体的化学方程式 .
①将此固体粉末加到水中,得到白色沉淀,且上层清液呈无色;
②该白色沉淀部分溶于稀硝酸,并有无色气体产生.由以上实验可推断:
(1)这包白色固体中,肯定存在
(2)写出②中产生无色气体的化学方程式
考点:物质的鉴别、推断,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的性质与用途
分析:根据题中明显的实验现象特征作为解题时的突破口:①中题眼有“上层溶液为无色”,“白色沉淀”;②中“白色沉淀部分溶于稀硝酸”中的“部分溶于”,产生“无色气体”,抓住这些题眼可快速解答.
解答:解:(1)①中“上层溶液为无色”可推得一定没有“CuSO4”;
“白色沉淀”有两种可能:原有的CaCO3或Na2SO4与BaCl2反应生成的硫酸钡.
②中“白色沉淀部分溶于稀硝酸”中的“部分溶于”可知白色沉淀既有“碳酸钙”,又有“硫酸钡”;而有硫酸钡时,则一定含有Na2SO4与BaCl2.但整个推断过程中,始终无法确定KNO3的存在与否.
所以,原固体粉末中一定含有CaCO3、Na2SO4和BaCl2,一定不含有CuSO4,可能含有KNO3.
故答案为:CaCO3、Na2SO4和BaCl2;CuSO4;
(2)②中产生无色气体是碳酸钙和硝酸反应产生硝酸钙和水和二氧化碳,故反应的方程式为:CaCO3+2HNO3═Ca(NO3)2+H2O+CO2↑.
“白色沉淀”有两种可能:原有的CaCO3或Na2SO4与BaCl2反应生成的硫酸钡.
②中“白色沉淀部分溶于稀硝酸”中的“部分溶于”可知白色沉淀既有“碳酸钙”,又有“硫酸钡”;而有硫酸钡时,则一定含有Na2SO4与BaCl2.但整个推断过程中,始终无法确定KNO3的存在与否.
所以,原固体粉末中一定含有CaCO3、Na2SO4和BaCl2,一定不含有CuSO4,可能含有KNO3.
故答案为:CaCO3、Na2SO4和BaCl2;CuSO4;
(2)②中产生无色气体是碳酸钙和硝酸反应产生硝酸钙和水和二氧化碳,故反应的方程式为:CaCO3+2HNO3═Ca(NO3)2+H2O+CO2↑.
点评:本题属于文字叙述型推断题,给出物质范围和实验现象,要求考生推出混合物中一定存在、一定不存在和可能存在的是什么物质;解答时以文字信息为序,寻找并抓住“题眼”,逐步分析“筛选”.这就要求考生熟悉这类题目的常见“题眼”,也就是解题的“突破口”;还必须熟练掌握常见物质的溶解性规律.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
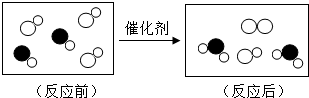 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )| A、此反应有单质生成 |
| B、原子在化学变化中是不可分的 |
| C、参加反应的两种分子的个数比为1:1 |
| D、此反应为置换反应 |