题目内容
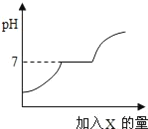
【题目】常温下,有些盐如CaCl2、NaCl等物质的水溶液呈中性;有些盐如Na2CO3等物质的水溶液呈碱性;有些盐如NH4Cl等物质的水溶液呈酸性。现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示。则X是( )
A. 水B. 澄清石灰水C. 纯碱溶液D. 稀盐酸
【答案】C
【解析】
由图可以看出,当加入X物质时,遇到盐酸会反应,之后随着盐酸的消耗,加入物质能够与氯化钙反应,但是对应生成物必须是中性的,而继续加入X,溶液显碱性,所以加入物质不能是碱,但是却显碱性。
A、HCl与CaCl2的混合溶液显酸性,加入水时溶液的pH升高,但是不会等于或大于7,故错误;
B、加入石灰水时,氢氧化钙能和盐酸反应生成氯化钙和水,溶液的pH升高。当酸完全被消耗之后,继续滴加石灰水,由于和氯化钙不反应,所以pH值马上大于7,而不会出现水平等于7的一段,故错误;
C、加入纯碱溶液时,碳酸钠能和盐酸反应,也能和氯化钙反应。开始时碳酸钠和盐酸反应,导致pH上升;当酸完全被消耗时,碳酸钠和氯化钙反应,生成物都是中性的,一直到氯化钙被完全消耗;当继续滴加碳酸钠时,由于碳酸钠显碱性,所以pH大于7,故正确;
D、加入盐酸时,盐酸和氯化钙不反应,溶液的pH不能等于或大于7,故错误。
故选C。

 名题金卷系列答案
名题金卷系列答案【题目】《天工开物》中记载的“倭铅”即是金属锌,说明我国炼锌在明代就出现。
探究一 用锌制取氢气甲同学拟用如图实验装置完成制取氢气和测量生成气体体积实验:
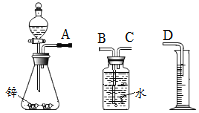
(1)写出锌与稀硫酸反应的化学方程式____。
(2)装置连接顺序是:A→___ →___→D(填字母)。
探究二 硫酸铜对氢气生成速率的影响
乙同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率,为此展开探究。
(设计实验)
在锥形瓶中分别放入足量的、等质量的、颗粒大小相同的锌粒,再向分液漏斗中加入由31.5%的稀硫酸,不同体积水、5%的硫酸铜溶液组成的混合液,试剂用量记录如下表:
混合液(试管编号) | ① | ② | ③ | ④ | ⑤ |
31.5%的H2SO4溶液/mL | 10 | V1 | 10 | 10 | 10 |
5%的CuSO4溶液/mL | 3.6 | 3.8 | 4.0 | 4.2 | 4.4 |
蒸馏水/mL | 16.4 | 16.2 | 16.0 | 15.8 | V2 |
收集70mL水所用时间/s | 21.20 | 20.45 | 19.69 | 20.49 | 21.33 |
(3)表中的V1=____mL,V2=____mL。
(分析与结论)
(4)表中____组反应速率最快,原混合液中H2SO4
探究三 锌与硫酸铜溶液反应
丙同学取打磨过的锌片按下表内容进行对比实验:
实验 项目 | 硫酸铜溶液 溶质质量分数 | 是否 添加稀硫酸 | 锌表面产生的现象 |
① | 1.6% | 否 | 黑色物质 |
② | 1.6% | 加2滴 | 红色物质,有极少量的气泡 |
③ | 8% | 否 | 红褐色物质 |
④ | 8% | 加2滴 | 光亮红色物质,有少量的气泡 |
⑤ | 16% | 否 | 红色物质,有极少量的气泡 |
⑥ | 16% | 加2滴 | 光亮红色物质,有较多气泡 |
(分析与结论)
(5)锌与硫酸铜溶液反应要产生红色的物质,需要的条件是___。
(6)根据第⑤组实验判断,硫酸铜溶液可能显___(选填:“酸”、“碱”或“ 中”)性。