题目内容
【题目】某工厂欲从只含有硫酸铜的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
回答下列问题:
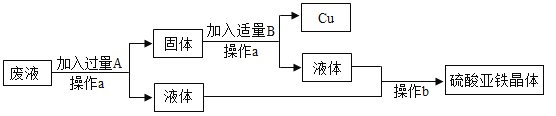
(1)操作a和操作b共同用到一种玻璃仪器是____,它在操作b中的作用____
(2)A、B物质的名称:A为_____,B为____
(3)A与废液主要成分反应的化学方程式为_____
(4)金属回收的意义____
【答案】玻璃棒 搅拌,防止局部温度过高,造成液体飞溅 铁粉 稀硫酸 Fe+CuSO4═FeSO4+Cu 节约金属资源等
【解析】
(1)操作a和操作b分别是过滤、蒸发操作,共同用到一种玻璃仪器是玻璃棒,它在操作b中的作用搅拌,防止局部温度过高,造成液体飞溅。
(2)从只含有硫酸铜的废液中回收金属铜,并得到工业原料硫酸亚铁,则A为铁粉,铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜;得到的固体B中含有铜和过量的铁,铁能与适量的稀硫酸反应生成硫酸亚铁溶液和氢气,则B为稀硫酸。
(3)A与废液主要成分反应,即铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu。
(4)回收废旧金属,可以节约金属资源和冶炼金属消耗的能源。
故答案为:
(1)玻璃棒,搅拌,防止局部温度过高,造成液体飞溅;
(2)铁粉;稀硫酸;
(3)Fe+CuSO4═FeSO4+Cu;
(4)节约金属资源等。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目