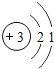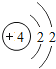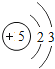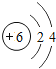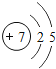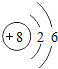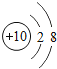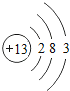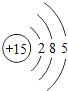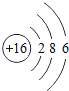题目内容
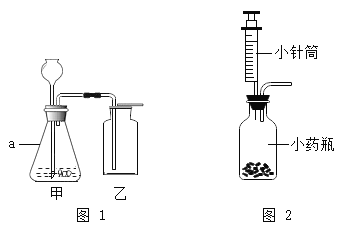
【题目】在实验室中常利用下列装置进行制取气体的实验,请回答下列问题:
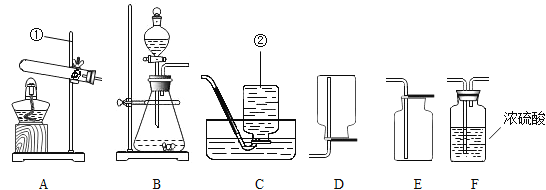
(1)写出标有序号的仪器名称:①____________,②__________________;
(2)实验室使用高锰酸钾制取并收集干燥的氧气,反应的化学方程式为______________,
所选装置的连接顺序:A →___________→______________(填装置代号)。该实验中还需对装置A进行的改进是_______________。若用 C 装置收集氧气,导管口开始有气泡放出时,不宜立即收集,应在_____时,开始收集气体;
(3)某同学想制取并收集二氧化碳气体,正确的装置是__________(填字母)。
【答案】铁架台或带铁夹的铁架台 集气瓶 ![]() F E 试管口放一团棉花 气泡连续均匀放出时 BE
F E 试管口放一团棉花 气泡连续均匀放出时 BE
【解析】
(1)据图可知仪器①是铁架台,②是集气瓶;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:![]() ;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,用向上排空气法收集的氧气比较干燥;氧气可以用浓硫酸干燥;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;
;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,用向上排空气法收集的氧气比较干燥;氧气可以用浓硫酸干燥;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热,可选装置B,二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,可选装置E。

 七彩题卡口算应用一点通系列答案
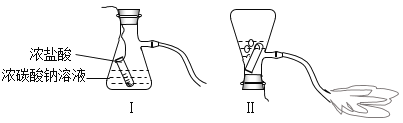
七彩题卡口算应用一点通系列答案【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究。
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想 1:废液中的溶质可能是 NaCl、Na2CO3和HCl。
猜想 2:废液中的溶质只有 NaCl。
猜想 3:废液中的溶质是 NaCl和HCl。
猜想 4:废液中的溶质是________。
(讨论与交流)
小明认为猜想1无需验证就知道是错误的,他的理由是________。
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现酚酞溶液不变色,于是小亮 认为猜想3正确。你认为他的结论_______(填“正确”或“错误”),理由是_______。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
__________ | ____________ | 猜想3正确 |
(2)验证猜想4,可选用的试剂有______。
A酚酞溶液
B氢氧化钾溶液
C稀硫酸
D氯化钡溶液。
(拓展与应用)
若废液中的溶质是 NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行______操作即可从废液中得到NaCl固体。
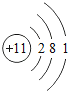
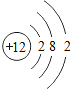
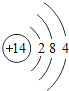
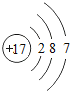
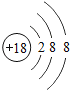
【题目】核电荷数为1﹣18的原子结构示意图等信息如下,请回答下列问题:
第一周期 | 1H
| 2He
| |||||||
第二周期 | 3Li
| 4Be
| 5B
| 6C
| 7N
| 8O
| 9F
| 10Ne
| |
第三周期 | 11Na
| 12Mg
| 13Al
| 14Si
| 15P
| 16S
| 17Cl
| 18Ar
| |
(1)不同种元素最本质的区别是_____(选填序号)
A质子数不同 B最外层电子数不同 C中子数不同 D相对原子质量不同
(2)在第三周期中,各原子结构的共同之处是_____;该周期中,各原子核外电子排布的变化规律是_____.
(3)在第三周期中,元素类型的变化情况是:从左到右由_____元素过渡到_____元素,并以稀有气体元素结尾.
(4)写出核外电子排布与氖原子相同的阳离子和阴离子各一个:阳离子_____,阴离子_____.
【题目】84消毒液是生活中常用的一种消毒液,主要成分为次氯酸钠(NaClO)。实验小组对其进行研究。
(查阅资料)
Ⅰ. NaClO溶液呈碱性。
Ⅱ.消毒杀菌的原理是使菌体蛋白质变性,变性程度越大,消毒液消毒杀菌效果越好。鸡蛋清中的蛋白质发生变性反应时变为白色固体物质。
Ⅲ.ORP指84消毒液的漂白能力,ORP数值越大,84消毒液的漂白能力越强。
(进行实验)
实验1:制备84消毒液
某同学制作了一种84消毒液发生器(如图所示),用石墨作电极,电解饱和氯化钠溶液,即可制得消毒液。

实验2:在鸡蛋清中加入不同浓度的消毒液,静置15min现象如下表。
序号 | 2-1 | 2-2 | 2-3 | 2-4 |
实验 操作 |
|
|
|
|
实验现象 | 液体表面产生大量气泡,无其他现象 | 液体中产生大量白色固体 | 液体中产生少量白色固体 | 液体中产生极少量白色固体 |
实验3:探究84消毒液漂白性的影响因素
序号 | 3-1 | 3-2 |
实验操作 | 取烧杯倒入30mL浓度为1:100的84消毒液,将烧杯放置在距离光源 10cm处进行光照,测量ORP变化 | 取四个烧杯,分别倒入30mL浓度为1:100的84消毒液,并置于20°C、30°C、40°C、50°C水浴中加热,测量 ORP变化 |
测量数据 |
|
|
(解释与结论)
(1)实验1中,发生的主要反应如下,补全①的化学方程式。
①2NaCl+2H2O![]() 2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
(2)实验2的目的是_______。
(3)实验3-1的结论是_______。
(4)根据实验3-2的测量数据可知,影响84消毒液漂白性的因素有_________。
(反思与评价)
(5)由实验3可知,84消毒液储存时需注意________。
(6)生活中,84消毒液不能与洁厕灵(主要成分是盐酸)混合使用的原因是________。