题目内容
【题目】用廉价金属回收贵重金属是工业生产中的一道重要程序。某化学兴趣小组的同学在实验室中进行了模拟实验。向含有硝酸铝和硝酸银的废液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣。下列说法正确的是( )
A.滤液中一定含有硝酸亚铁,滤渣中一定含有银
B.滤液质量比反应前原溶液质量大
C.滤液中最少只含有一种溶质
D.若反应后所得滤液呈浅绿色,则滤渣中一定含有铁、银
【答案】A
【解析】
向含有硝酸铝和硝酸银的废液中加入一定量的铁粉,铁粉和硝酸银反应生成硝酸亚铁和银,铁粉和硝酸铝不反应。当铁粉少量时,不能将银全部置换出来,则滤渣中只有银,滤液中有硝酸银、硝酸铝和硝酸亚铁;当铁粉过量时,铁将银全部置换出来,则滤渣中有银和铁,滤液中有硝酸亚铁和硝酸铝。
A. 根据分析可知,滤液中一定含有硝酸亚铁,滤渣中一定含有银,符合题意;
B. 根据分析可知,该过程的化学反应方程式为:![]() ,溶液溶质每340份质量的硝酸银变为180份质量的硝酸亚铁,所以溶质质量减小,溶液质量减小,不符合题意;
,溶液溶质每340份质量的硝酸银变为180份质量的硝酸亚铁,所以溶质质量减小,溶液质量减小,不符合题意;
C. 根据分析可知,滤液中最少含有两种溶质,不符合题意;
D. 若反应后所得滤液呈浅绿色,说明滤液中有硝酸亚铁,滤渣中一定含有银,不一定含有铁,不符合题意。故选A。

【题目】某化学实验小组在做“从 NaCl 和Na2CO3的混合物中提纯 NaCl”的实验。同学们经过讨论认为利用两物质化学性质的差异,可采用如下化学方法来提纯。
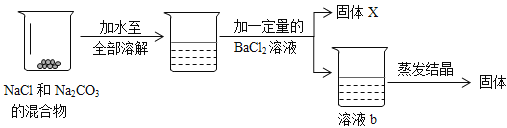
(1)如图 X 的化学式为_______________。由于BaCl2溶液的用量不易控制,会使溶液 b 的溶质有多种情况,导致蒸发后得到的固体可能不纯。
(2)实验结束后同学们对溶液 b 的溶质成分进行探究。
(作出猜想)猜想一:NaCl、BaCl2
猜想二:NaCl
猜想三:___________________。
(设计方案)经讨论,大家认为只用一种试剂就能作出判断.
实验步骤 | 实验现象 | 实验结论 |
取少量溶液 b 于试管中,向其中加入_____________。 | 若_______ | 猜想一正确 |
若_______ | 猜想二正确 | |
若_______ | 猜想三正确 |
各组依据上述设计方案进行了实验,验证了反应后溶质的确有三种情况。
(3)(反思评价)大家认为用物理方法和化学方法都可以实现物质的提纯。用化学方法提纯还要考虑到______对提纯效果的影响。
(4)(拓展提升)老师说:“合理选择试剂,用化学方法可以从 NaCl 和Na2CO3的混合物中提纯NaCl,方法是向混合物中加入过量的_____________,充分反应后,经蒸发结晶就能得到 NaCl。