题目内容
【题目】84消毒液是生活中常用的一种消毒液,主要成分为次氯酸钠(NaClO)。实验小组对其进行研究。
(查阅资料)
Ⅰ. NaClO溶液呈碱性。
Ⅱ.消毒杀菌的原理是使菌体蛋白质变性,变性程度越大,消毒液消毒杀菌效果越好。鸡蛋清中的蛋白质发生变性反应时变为白色固体物质。
Ⅲ.ORP指84消毒液的漂白能力,ORP数值越大,84消毒液的漂白能力越强。
(进行实验)
实验1:制备84消毒液
某同学制作了一种84消毒液发生器(如图所示),用石墨作电极,电解饱和氯化钠溶液,即可制得消毒液。
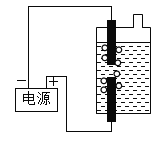
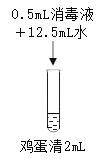
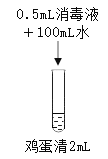
实验2:在鸡蛋清中加入不同浓度的消毒液,静置15min现象如下表。
序号 | 2-1 | 2-2 | 2-3 | 2-4 |
实验 操作 |
|
|
|
|
实验现象 | 液体表面产生大量气泡,无其他现象 | 液体中产生大量白色固体 | 液体中产生少量白色固体 | 液体中产生极少量白色固体 |
实验3:探究84消毒液漂白性的影响因素
序号 | 3-1 | 3-2 |
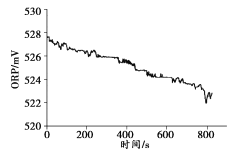
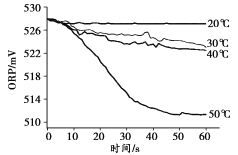
实验操作 | 取烧杯倒入30mL浓度为1:100的84消毒液,将烧杯放置在距离光源 10cm处进行光照,测量ORP变化 | 取四个烧杯,分别倒入30mL浓度为1:100的84消毒液,并置于20°C、30°C、40°C、50°C水浴中加热,测量 ORP变化 |
测量数据 |
|
|
(解释与结论)
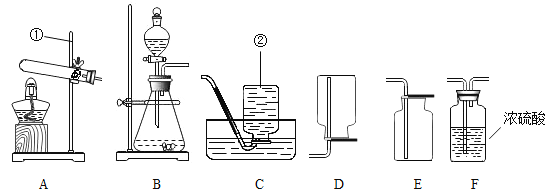
(1)实验1中,发生的主要反应如下,补全①的化学方程式。
①2NaCl+2H2O![]() 2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
(2)实验2的目的是_______。
(3)实验3-1的结论是_______。
(4)根据实验3-2的测量数据可知,影响84消毒液漂白性的因素有_________。
(反思与评价)
(5)由实验3可知,84消毒液储存时需注意________。
(6)生活中,84消毒液不能与洁厕灵(主要成分是盐酸)混合使用的原因是________。
【答案】H2 探究不同浓度的84消毒液的消毒杀菌效果 光照时间越长,84消毒液的漂白能力越弱 温度 避光、低温 二者会发生化学反应
【解析】
(1)根据质量守恒定律可知,化学反应前后原子的个数相同。则反应前有2个钠原子、2个氯原子、4个氢原子、2个氧原子,反应后有2个钠原子、2个氧原子、2个氯原子,相差2个氢原子,则补充的物质为氢气。故答案为:H2;
(2)实验2中,鸡蛋清均为2mL,但是消毒剂和水的比例不同。根据控制变量的实验思想,可以分析出,实验2中的四组实验的变量为消毒剂的浓度,则该实验的目的是为了探究不同浓度的84消毒液的消毒杀菌效果。故答案为:探究不同浓度的84消毒液的消毒杀菌效果;
(3)通过实验3-1的图像分析可知,随着光照时间的增长,ORP值在逐渐降低。根据题干的信息可知, ORP值是定量描述84消毒液的漂白能力的数值,数值越大,漂白能力越强。则可以得出结论,光照的时间越久,ORP值越低,则84消毒液的漂白能力越差。故答案为:光照时间越长,84消毒液的漂白能力越弱;
(4)通过实验3-2的数据可知,温度越高,水浴时间越长,则84消毒剂的漂白能力越弱。则可以得出,84消毒液的漂白能力与温度有关。故答案为:温度;
(5)通过实验3-1的图像分析可知,光照时间越久,84消毒液的漂白能力越弱。通过实验3-2的数据可知,温度越高,水浴时间越长,则84消毒剂的漂白能力越弱。则可以分析出,影响84消毒液的漂白能力的因素有温度、光照时间。所以在保存时,应该避光并低温。故答案为:避光、低温;
(6)根据资料可知,84消毒液的主要成分是次氯酸钠,水溶液呈碱性。而盐酸的水溶液呈酸性。两种物质混合后,会发生化学反应,从而使84消毒液的效力降低。故答案为:二者会发生化学反应。

【题目】某化学实验小组在做“从 NaCl 和Na2CO3的混合物中提纯 NaCl”的实验。同学们经过讨论认为利用两物质化学性质的差异,可采用如下化学方法来提纯。

(1)如图 X 的化学式为_______________。由于BaCl2溶液的用量不易控制,会使溶液 b 的溶质有多种情况,导致蒸发后得到的固体可能不纯。
(2)实验结束后同学们对溶液 b 的溶质成分进行探究。
(作出猜想)猜想一:NaCl、BaCl2
猜想二:NaCl
猜想三:___________________。
(设计方案)经讨论,大家认为只用一种试剂就能作出判断.
实验步骤 | 实验现象 | 实验结论 |
取少量溶液 b 于试管中,向其中加入_____________。 | 若_______ | 猜想一正确 |
若_______ | 猜想二正确 | |
若_______ | 猜想三正确 |
各组依据上述设计方案进行了实验,验证了反应后溶质的确有三种情况。
(3)(反思评价)大家认为用物理方法和化学方法都可以实现物质的提纯。用化学方法提纯还要考虑到______对提纯效果的影响。
(4)(拓展提升)老师说:“合理选择试剂,用化学方法可以从 NaCl 和Na2CO3的混合物中提纯NaCl,方法是向混合物中加入过量的_____________,充分反应后,经蒸发结晶就能得到 NaCl。
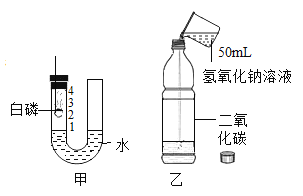
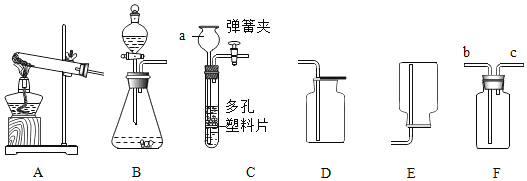
【题目】请从A~D中任选三个实验作答,若均做答,按前三个计分。如下图,在一只集气瓶(或广口瓶)中进行实验。回答相关问题。
序号 | 步骤 | 问题 |
A | ①收集一瓶氧气②伸入燃着的木炭③倒入澄清石灰水并振荡 | 该实验的目的是_______。 |
B | ①收集二氧化碳②倒入氢氧化钠溶液振荡③…… | 该实验探究CO2能否与NaOH反应,步骤③的操作是______。 |
C | ①倒入10%的H2O2溶液②伸入带火星的木条③加入少量MnO2 | 实验的结论是__________。 |
D | ① 放入燃着的蜡烛②放入少量碳酸钙粉末③加入适量盐酸 | 观察到的现象是_______。 |