题目内容
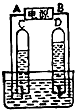 阿伏加德罗曾经总结出下列一条定律:“在同温同压下,同体积的任何气体都含有相同数量的分子.”请看图简易电解水的装置,回答下列问题:?
阿伏加德罗曾经总结出下列一条定律:“在同温同压下,同体积的任何气体都含有相同数量的分子.”请看图简易电解水的装置,回答下列问题:?(1)指出电源的“正”、“负”极.?
A为
(2)C管中产生的是
(3)写出水电解的化学方程式(或文字表达式、符号表达式):
考点:电解水实验,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:在电解水实验中,可观察到的现象有:正极的气体体积少,能使带火星的木条复燃,负极的气体体积多,能燃烧,而且体积多的是少的二倍.根据以上现象可推出正极产生的气体是氧气,负极产生的气体是氢气,还能进一步推出水由氢元素和氧元素组成.
解答:解:(1)由电解水的实验装置可知,C试管收集的气体较多是氢气,是电源的负极产生的气体,故A为负极;D试管收集的气体较少是氧气,是电源的正极产生的气体,故B为正极.?
(2)由上述分析可知,C管中产生的是氢气,D管产生的是氧气.C、D两管中气体的体积比为2:1,由于在同温同压下,同体积的任何气体都含有相同数量的分子所以,所以,分子个数之比是2:1.
(3)电解水生成了氢气和氧气,反应的化学方程式是:2H2O
2H2↑+O2↑,由上面的实验事实得出结论:说明水是由氢元素、氧元素组成的.?
故答为:(1)负,正;?(2)氢气,氧气.2:1,2:1; (3)2H2O
2H2↑+O2↑,氢元素、氧元素.?
(2)由上述分析可知,C管中产生的是氢气,D管产生的是氧气.C、D两管中气体的体积比为2:1,由于在同温同压下,同体积的任何气体都含有相同数量的分子所以,所以,分子个数之比是2:1.
(3)电解水生成了氢气和氧气,反应的化学方程式是:2H2O
| ||
故答为:(1)负,正;?(2)氢气,氧气.2:1,2:1; (3)2H2O
| ||
点评:本题就考查的内容不难,但是根据题中信息进行合理的推导得出结论,相对要难一些,这是一种能力题,同学们要学会读题提取有用的信息.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
根据如图提供的信息,下列判断不正确的是( )
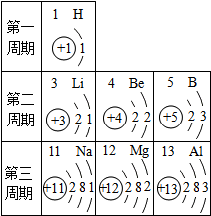

| A、元素所在的周期数等于其原子的电子层数 |
| B、钠离子核处有两个电子层 |
| C、第二、三周期元素的原子从左至右最外层电子数逐渐增多 |
| D、在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+2 |
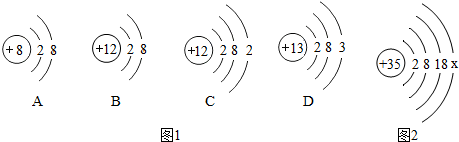
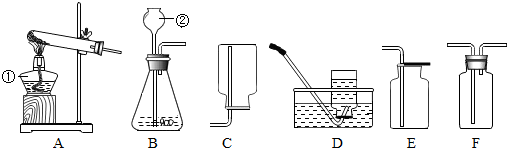
 课题小组为测定某黄铜样品中铜的含量,取20g黄铜样品放在烧杯中,然后向其中注入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参与反应).随反应进行,注入稀盐酸的质量与反应得到气体的质量呈右图所示关系.请完成下列计算内容:
课题小组为测定某黄铜样品中铜的含量,取20g黄铜样品放在烧杯中,然后向其中注入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参与反应).随反应进行,注入稀盐酸的质量与反应得到气体的质量呈右图所示关系.请完成下列计算内容: