题目内容
根据图1四种粒子的结构示意图,完成以下填空:
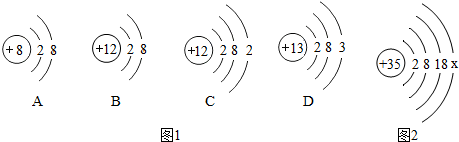
(1)属于阴离子结构的粒子是 (填化学符号).
(2)某元素R形成的一种钠盐的化学式为NaRO2,则R的原子结构示意图可能是 (填字母).
(3)图2中X= ,属于 元素(填“金属”或“非金属”).

(1)属于阴离子结构的粒子是
(2)某元素R形成的一种钠盐的化学式为NaRO2,则R的原子结构示意图可能是
(3)图2中X=
考点:原子结构示意图与离子结构示意图,化学符号及其周围数字的意义
专题:化学用语和质量守恒定律
分析:(1)阳离子:核内质子数>核外电子数,阴离子:核内质子数<核外电子数;
(2)根据氧化物为R2O3来确定R的化合价,元素的最高正价=最外层电子数;
(3)在原子结构示意图中,圆圈内数字为核内质子数,等于核外的电子数,等于原子序数;根据原子序数判断元素,根据最外层电子数判断元素的种类,非金属元素的最外层电子数一般多余4个.
(2)根据氧化物为R2O3来确定R的化合价,元素的最高正价=最外层电子数;
(3)在原子结构示意图中,圆圈内数字为核内质子数,等于核外的电子数,等于原子序数;根据原子序数判断元素,根据最外层电子数判断元素的种类,非金属元素的最外层电子数一般多余4个.
解答:解:
(1)阴离子结构:质子数<电子数,题中核内质子数<核外电子数的即为阴离子,只有A,故答案为:A;
(2)根据化合价规则,因为氧元素的化合价为-2,钠元素的化合价为+1,根据化合物中元素正负化合价的代数和为零,所以R元素的化合价为+3,即最外层电子数为3,故答案为:D.
(3)由原子结构示意图可知,图中X=35-2-8-18=7;根据原子结构示意图的特点:非金属元素的最外层电子数一般多于4,由原子结构示意图判断:该元素属于非金属元素;
答案:
(1)A
(2)D
(3)7 非金属
(1)阴离子结构:质子数<电子数,题中核内质子数<核外电子数的即为阴离子,只有A,故答案为:A;
(2)根据化合价规则,因为氧元素的化合价为-2,钠元素的化合价为+1,根据化合物中元素正负化合价的代数和为零,所以R元素的化合价为+3,即最外层电子数为3,故答案为:D.
(3)由原子结构示意图可知,图中X=35-2-8-18=7;根据原子结构示意图的特点:非金属元素的最外层电子数一般多于4,由原子结构示意图判断:该元素属于非金属元素;
答案:
(1)A
(2)D
(3)7 非金属
点评:本题考查学生微粒的结构示意图知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
下列有关粒子的叙述中正确的是( )
| A、分子是保持物质性质的最小粒子 |
| B、原子是最小的粒子,不可以再分 |
| C、氯化钠是由离子直接构成的物质 |
| D、分子之间有间隔,而原子之间没有间隔 |
用酒精灯给试管里的液体加热时,造成试管破裂,可能的原因有:①用酒精灯外焰加热;②试管外壁有水;③试管底部接触灯芯;④试管内的液体超过试管容积的三分之二;⑤没有进行预热就直接集中加热试管内的液体.你认为原因可能是( )
| A、①③⑤ | B、②④ |
| C、②③⑤ | D、③④ |
下列粒子结构示意图中,表示阴离子的是 ( )
A、 |
B、 |
C、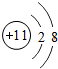 |
D、 |
某同学用量筒量取液体时,俯视液面读数为40mL,倒出部分液体后,仰视液面读数为20mL,则倒出的液体体积为( )
| A、大于20mL |
| B、等于20mL |
| C、小于20mL |
| D、无法判断 |
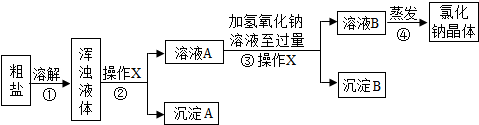

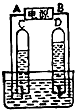 阿伏加德罗曾经总结出下列一条定律:“在同温同压下,同体积的任何气体都含有相同数量的分子.”请看图简易电解水的装置,回答下列问题:?
阿伏加德罗曾经总结出下列一条定律:“在同温同压下,同体积的任何气体都含有相同数量的分子.”请看图简易电解水的装置,回答下列问题:?