题目内容
【题目】酸、碱、盐、燃料等是我们学过的重要物质,请根据相关知识回答下列问题:
(1)稀盐酸能除铁锈(铁锈的主要成分是Fe2O3),写出稀盐酸除铁锈的反应方程式_____。
(2)现有:NaOH溶液、Ba(NO3)2溶液、Na2CO3溶液、CuSO4溶液、稀硫酸,从以上5种物质中选出一种碱溶液与一种盐溶液反应并写出化学方程式_____________。
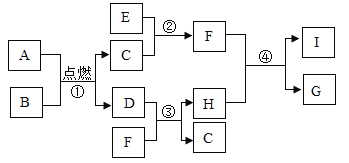
(3)天然气是一种重要的燃料,其主要成分为甲烷(CH4)。某课外兴趣小组同学对甲烷在氧气中完全燃烧后的产物进行探究。
①提出假设:A同学假设只生成CO2,B同学假设只生成H2O,有同学认为A、B同学的假设都不完全正确,请你提出合理的猜想_________。
②实验验证:为了验证你的猜想,可以将甲烷完全燃烧的产物依次通过____________、进行检验(填物质名称)。
【答案】Fe2O3 + 6HCl═ 2FeCl3 +3H2O 2NaOH + CuSO4 ═Cu(OH)2↓+Na2SO4 生成CO2和H2O 无水硫酸铜、澄清石灰水
【解析】
稀盐酸和氧化铁反应生成氯化铁和水,氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠,无水硫酸铜检验是否有水生成,澄清石灰水检验是否有二氧化碳生成。
(1)稀盐酸能除铁锈(铁锈的主要成分是Fe2O3),稀盐酸除铁锈的反应方程式为![]() 。
。
(2)NaOH溶液、Ba(NO3)2溶液、Na2CO3溶液、CuSO4溶液、稀硫酸,碱溶液是氢氧化钠溶液、能和氢氧化钠反应的盐溶液是CuSO4溶液,反应并写出化学方程式![]() 。
。
(3)①A同学假设只生成CO2,B同学假设只生成H2O,故应该假设生成CO2和H2O两种物质。
②甲烷完全燃烧的产物是水和二氧化碳,为了验证猜想,可以将甲烷完全燃烧的产物依次通过无水硫酸铜检验水,如果变蓝色,说明生成了水;通过澄清石灰水检验二氧化碳,如果变浑浊,说明有二氧化碳生成。

【题目】某兴趣小组对石灰石样品进行如下实验取12g样品放入烧杯中,将100g稀盐酸分4次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
1 | 2 | 3 | 4 | |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 8 | 4 | 2 | 2 |
(1)样品中碳酸钙的质量为_________g:
(2)所用稀盐酸中溶质的质量分数_____。(写出计算过程)