题目内容
实验室测定一瓶稀硫酸中溶质的质量分数。取10g该待测液,向其中逐滴加入5%的NaOH溶液,加入NaOH溶液的质量与溶液pH的变化关系如图所示。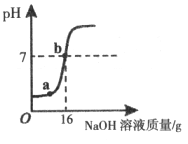
(1)16g 5%的NaOH溶液中所含溶质的质量是________g。
(2)a点对应溶液中的溶质是________________。
(3)计算待测稀硫酸中溶质的质量分数(写出计算过程及结果)。
(1)0.8 g
(2)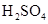 和
和
(3) 9.8%
解析试题分析:由图可知当加入氢氧化钠溶液的质量为16g时,溶液的PH=7(b点),即氢氧化钠与硫酸恰好完全反应; 在a点时,溶液的PH<7,即硫酸过量,此时溶液中的溶质有过量的硫酸和生成的硫酸钠;利用化学方程式,根据氢氧化钠的质量可求出稀硫酸中溶质的质量,再除以稀硫酸的质量即可求出溶质的质量分数。
(1)16g 5%的NaOH溶液中所含溶质的质量="16g×" 5%=0.8g
(3)[解]设待测稀硫酸中溶质的质量为x。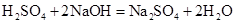
98 80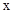 0.8g
0.8g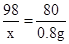
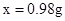
待测稀硫酸中溶质的质量分数=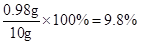
答:待测稀硫酸中溶质的质量分数是9.8%。
考点:溶质质量分数的计算、利用化学方程式的计算

 中考解读考点精练系列答案
中考解读考点精练系列答案(6分)课外活动时,同学们采用以下两种方法测定某氯化钠溶液的溶质质量分数。
(1)【化学方法】向一定量氯化钠溶液中加入足量硝酸银溶液,得到2.87g氯化银固体,则该氯化钠溶液中氯化钠的质量为多少?(根据化学方程式列式计算)
经多次实验测定,该溶液的溶质质量分数为10%。
(2)【物理方法】取一定量该溶液进行蒸发,测量实验数据如下:
| 蒸发皿的质量(g) | 25.0 |
| 蒸发皿+食盐溶液(g) | 45.0 |
| 蒸发皿+食盐晶体(g) | 27.4 |
| 数据处理 | 溶液的溶质质量分数为 |
A.蒸发时未用玻璃棒搅拌 B.所取氯化钠溶液质量较大
C.蒸发时出现少量晶体时就停止加热 D.实验后未将玻璃棒上的白色固体移入蒸发皿
有一种石灰石样品的成分是CaCO3和SiO2。课外小组同学将100g盐酸分5次加入到35g该石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图像:
| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
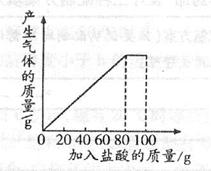
请计算:
(1)第2次加入盐酸后,a为 g;
(2)石灰石样品中碳酸钙的质量分数;(计算结果精确至0.1%)
(3)10%的CaCl2溶液可做路面保湿剂。欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)(计算结果精确至0.1g)