题目内容
【题目】如图是某化学反应的微观模拟示意图,根据该图判断,下列说法中正确的是( )
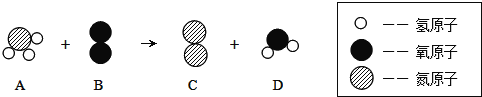
A. 反应前后原子种类均发生改变 B. 该反应是置换反应
C. 生成的C与D质量比为14:27 D. 参加反应的两种物质分子个数比为4:1
【答案】BC
【解析】
观察微观模拟示意图,分析反应物、生成物,写出反应的化学方程式,据其意义分析判断有关的问题。
由微观过程图可知,反应的化学方程式应该是:4NH3+3O2=2N2+6H2O.A、根据微观示意图可知,反应前后原子的种类没有发生变化,只是原子重新组合,选项错误;B、由化学方程式可知,该反应是单质和化合物反应产生新的单质和新的化合物,属于置换反应,选项正确;C、反应生成的氮气与水的质量之比为:(2×28):(6×18)=14:27,选项正确;D、由化学方程式可知,参加反应的A和B的分子个数比为4:3,选项错误。故选BC。

【题目】FeCl3(氯化铁)溶液也能对过氧化氢的分解能起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响。
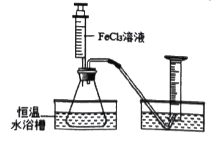
Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,通过观察______,就可以粗略判断,得到实验结果,为进一步判断上述试验结论的准确性,运用图示装置,小刚同学进行了如下实验方案设计进行定量研究。
Ⅱ.[方案一]在不同过氧化氢浓度下,测定收集相同体积气体所需的时间。
[方案二]在不同过氧化氢浓度下,测定_________。
方案二的实验测量结果:
物理量 序号 | H2O2溶液的浓度和体积 | 2% FeCl3溶液的 体积(mL) | 反应的时间 ( min) | 生成O2的体积 (mL) |
1 | 30%,10mL | x | 5 | V1 |
2 | 10%,10mL | 3 | y | V2 |
(1)表中x=_________,y=_______。
(2)通过测量,若V1_______V2(填“>”、“=”或“<”) 得出的实验结论为_____。
【题目】某同学想定量测定某红色粉末中氧化铁的质量分数,进行如下实验:
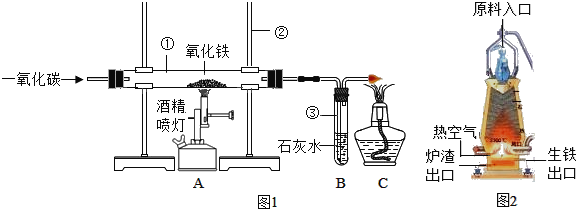
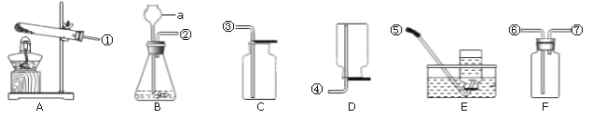
(1)图1是实验室模拟炼铁的装置图,试回答
实验步骤:按上图连接实验装置、 _______、装药品、固定实验装置后,剩下的主要实验步骤有:①通入一氧化碳;②停止通入一氧化碳;③点燃酒精灯;④熄灭酒精灯;⑤点燃酒精喷灯;⑥熄灭酒精喷灯.正确的操作顺序是(填序号)__________.
(2)实验过程中,仪器①中的现象___________,所发生反应的化学方程式是_________仪器③中所发生反应化学方程式是_______。
(3)请写出证明产物中含铁粉的一种化学方法:____________.
(4)实验过程中产生的尾气不能直接排放的原因是____________.请从节能的角度出发,对于尾气处理,你有什么好的建议:____________
(5)定量测定该红色粉末中氧化铁的质量分数
某同学称取该红色粉末5.0g装入硬质玻璃管中,完全反应后,称量相关物质的总质量其数据如下表:
反应前 | 反应后 |
玻璃管和红色粉末总质量 48.3g | 玻璃管和固体物质总质量47.1g |
根据上述表格中的实验数据计算:红色粉末中氧化铁的质量分数为____.(写出计算过程,)
(6)如图2是工业生产中炼铁高炉的结构图.实际生产中炼铁的原料有铁矿石、热空气、石灰石、以及_____________;该物质有两个作用,第一个作用提供能量,另一个作用是__________;生铁出口低于炉渣出口的原因是_________。