题目内容
【题目】我们通过学习知道,钠原子在化学反应中易失去电子,成为钠离子.
(1)“在金属活动顺序里,位于前面的金属能把位于后面的金属从其盐溶液里置换出来”,金属钠排在金属铜的前面。有的同学据此推测:钠能从蓝色硫酸铜溶液中把铜置换出来。
教师按照下列顺序进行演示实验,并记录实验现象:
步骤一:将硫酸铜溶液倒入培养皿中
步骤二:用镊子将一小块金属钠放入培养皿中
现象1:金属钠成小球状在液体表面游动
现象2:金属小球逐渐变小至消失,在小球游动的轨迹下面只有蓝色絮状难溶物出现
①由以上实验现象得出结论:因为反应中没有____色的物质 生成,所以金属钠_____________________(填:“能” 或“不能”)把铜从硫酸铜溶液中置换出来。
②对实验涉及的物质进行分析:硫酸铜溶液中溶剂为水,溶质为_______________(填化学式),钠与硫酸铜溶液反应后培养中皿所含元素有: Na、 Cu、 H、O、______________________ (填元素 符号)五种元素。查阅资料得知:“ 蓝色絮状难溶物”是一种学过的碱,该物质的名称是_________________________。
(2)有的同学又产生新的疑问:钠能否与水发生反应?生成物是什么?教师为解答学生的疑惑,又设计并进行如下实验。同时记录有关现象:
步骤一:向盛有蒸馏水的烧杯中滴入几滴酚酞试液并搅拌均匀
步骤二:用镊子将一小块金属钠放入烧杯中
现象:钠在液体表面成小球状游动并发出“嘶嘶”声响。小球周围有“蒸汽”产生,有时有火星出现,液体中出现红色。
请结合上面所示信息,回答下列问题:
①用手触摸反应后烧杯外壁,感觉烫手,说明钠与水发生的是____ (填:“吸 热”或“放热”)反应。
②从现象中可以断定:液体中出现红色说明反应后液体显_______________________性,结合液体中所含元素,继而推断有_______________________(填化学式)生成。另外,钠与水反应还生成一种可燃性气体单质。请写出钠与水反应的化学方程式:________________________。
【答案】红 不能 CuSO4 S 氢氧化铜 放热 碱 NaOH ![]()
【解析】
(1)①如果钠能将铜从硫酸铜溶液中置换出来,则应有红色的铜产生,由以上实验现象得出,反应中没有红色的物质生成,所以金属钠不能把铜从硫酸铜溶液中置换出来;
②对实验涉及的物质进行分析:硫酸铜溶液中溶剂为水,溶质为硫酸铜,化学式为CuSO4;
根据质量守恒定律,化学反应前后元素的种类、数目不变,故钠与硫酸铜溶液反应后培养皿中所含元素有: Na、 Cu、 H、O、S五种元素,“ 蓝色絮状难溶物”是一种学过的碱,该物质的名称是氢氧化铜;
(2)①用手触摸反应后烧杯外壁,感觉烫手,说明钠与水发生的是放热反应;
②酚酞遇碱变红,故液体中出现红色说明反应后液体显碱性,结合液体中所含元素(Na、H、O),继而推断有NaOH生成。另外,钠与水反应还生成一种可燃性气体单质,由所含元素可推出该可燃性气体单质为氢气,故钠与水反应的化学方程式:![]() 。
。

【题目】图为某小组探究金属化学性质的两组实验。
实验I | 实验Ⅱ |
|
|
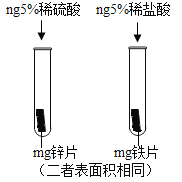
(1)实验Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是______________,请你写出A试管中发生反应的化学方程式_________________。
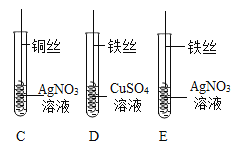
(2)写出实验Ⅱ中C试管内发生反应的化学方程式_________________,D实验中观察到的现象是_____________。
(3)实验Ⅱ中要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是________(填序号),由此判断出三种金属的活动性由强到弱的顺序是________________。