题目内容
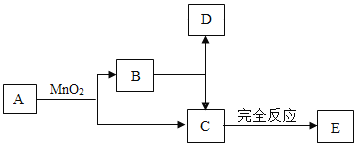
【题目】已知A、B、C、D、E五种物质之间存在以下的转化关系,其中A、B两种物质的组成元素相同,且常温下都是液态;D是最理想的燃料;E是空气成分之一。试回答:
(1)写出A物质的化学式_____。
(2)D作为最理想的燃料,突出的优点是_____。
(3)写出实验室制取C的化学方程式_____。
【答案】H2O2 燃烧产物为水,有利于环境保护 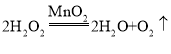
【解析】
D是最理想的燃料,可推出D是氢气,A、B两种物质的组成元素相同,且常温下都是液态,A可在MnO2的存在下生成B与C,可推出A为H2O2,B为H2O,C为O2。
(1)A物质为过氧化氢,化学式为H2O2;
(2)D作为最理想的燃料,突出的优点是:D是氢气,氢气燃烧的产物只有水,可以保护环境;
(3)C为氧气,则实验室制取氧气的化学方程式为: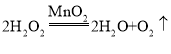 或者
或者![]() 或者
或者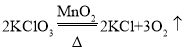

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
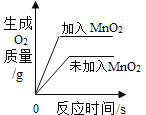
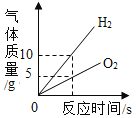
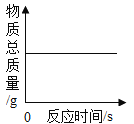
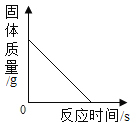
【题目】下列图象能正确反映对应关系的是( )
|
|
|
|
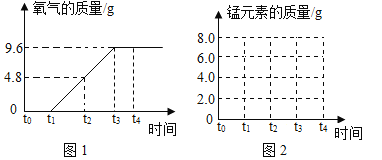
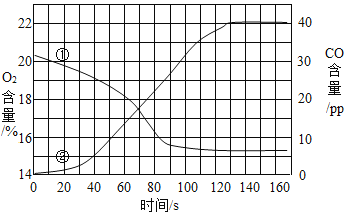
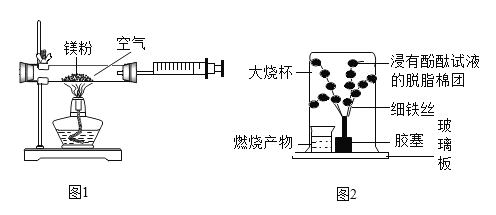
A.用等质量、等浓度的过氧化氢溶液制取氧气 | B.将水通电一段时间 | C.一定质量的红磷在密闭容器中燃烧 | D.加热一定质量的氯酸钾制氧气 |
A. A B. B C. C D. D