题目内容
【题目】酸、碱、盐在生产生活中具有广泛的用途。化学实验室中有失去标签的四瓶无色溶液:稀盐酸、氢氧化钙溶液、碳酸钠溶液、酚酞试液,现将其任意编号为A、B、C、D.然后两两组合进行实验,其中部分现象如下表,请回答:
实验 | A+B | A+C | B+C | B+D |
现象 | 溶液变红 | 溶液变红 | 产生沉淀 | 产生气体 |
(1)配酞试液是____________(填编号);
(2)B与C反应的化学方程式为____________________。
(3)写出D的一种用途:____________________。
【答案】A ![]() 金属除锈(或制某些药物;或在胃中帮助消化等)
金属除锈(或制某些药物;或在胃中帮助消化等)
【解析】
酚酞遇碱性溶液变红,氢氧化钙溶液、碳酸钠溶液显碱性,滴加酚酞会变红色,A+B以及A+C都变红色,故A为酚酞,B和C为氢氧化钙或者碳酸钠,故D为稀盐酸,B+D生成气体,故B为碳酸钠,C为氢氧化钙,代入实验,符合题意。
(1)酚酞遇碱性溶液变红,氢氧化钙溶液、碳酸钠溶液显碱性,滴加酚酞会变红色,A+B A+C都变红色,故A为酚酞,故填:A。
(2)由分析可知B为碳酸钠C为氢氧化钙反应生成碳酸钙和氢氧化钠,故填;![]() 。
。
(3)由分析可知D为稀盐酸,可用于除锈,故填:金属除锈。

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
【提出问题】 化学反应前后各物质的质量总和是否相等?
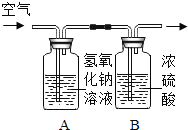
【查阅资料】 氢氧化钠溶液可以吸收二氧化碳气体
【猜想与假设】 猜想1:不相等;猜想2:相等。
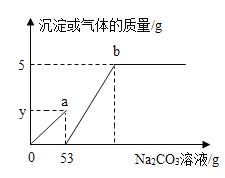
【实验探究】 甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生,天平指针向右偏转 | _________,天平指针没有偏转 |
结论 | 猜想1正确,反应的化学方程 式:_______________. | 猜想2正确 |
【反思评价】 究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_______________中进行。
【优化装置】 同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是(填序号)___,从另外两种装置中任选一种指出其不足:________。
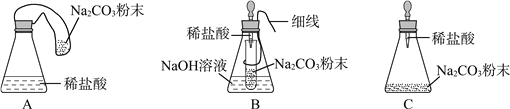
【得出结论】 同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步
分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论:_________________________的各物质的质量总和等于反应后生成的各物质的质量总和。
【解释应用】
解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由_________种元素组成。
【题目】氯酸钾在工业上用于制造焰火、漂白剂等,在实验室可用于制造氧气。工业上利用石灰浆制备氯酸钾的流程是:

(1)写出实验室用氯酸钾制取氧气的化学方程式____________________。
(2)在实验室里,“操作a”中需要用到玻璃棒,其作用是__________。
(3)“反应1”的化学反应方程式为:6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6X,Ca(ClO3)2的名称是__________,X的化学式为__________。
(4)下表是有关物质常温下的溶解度。
物质 | KCl | CaCl2 | KClO3 | Ca(ClO3)2 |
溶解度/g | 34.2 | 74.5 | 7.3 | 209.0 |
“反应2”为复分解反应,参看表中溶解度,写出该反应的化学方程式__________。
(5)上述石灰浆可由电石(CaC2)与水反应制得。现有某电石渣,其中含氢氧化钙92.5%,用该电石渣处理含硫酸49Kg的酸性废水(假设电石渣中的杂质、废水中其他成分均不参加反应),需要电石渣的质量是__________kg。