题目内容
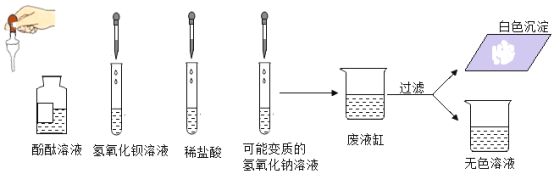
【题目】下图是某实验小组对氢氧化钠部分性质的探究过程:
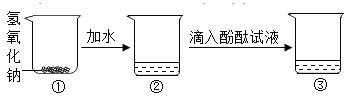
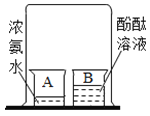
小红用手触摸烧杯②的外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会_______(填“吸热"或“放热”),烧杯③的溶液呈_________色。
小红取烧杯③中的适量溶液于试管中,滴加稀盐酸后振荡,溶液呈无色,于是她认为氢氧化钠与稀盐酸恰好完全反应。该反应的化学方程式为________。
小明不同意她的观点,理由是如果稀盐酸过量,溶液也呈无色。
[提出问题]氢氧化钠与稀盐酸是否恰好完全反应呢?
[实验探究]
方案 | 方案一 | 方案二 | 方案三 |
实验操作 | 用洁净的玻璃棒蘸取反应后溶液,滴到pH试纸上,将试纸显示的颜色与标准比色卡比较 | 取适量反应后溶液于试管中,滴加AgNO3溶液 | 取适量反 应后溶液于试管中,滴加Na2CO3溶液 |
实验现象 | 试纸变为红色,pH______7 | 有_______生成 | 有气泡冒出 |
实验结论 | 稀盐酸过量 | 稀盐酸过量 | 稀盐酸过量 |
[得出结论]氢氧化钠与稀盐酸没有恰好完全反应。
[交流讨论]同学们经讨论,发现上述三个方案中有一个不能达到探究目的,它是方案_______,理由是________。
【答案】放热 红 ![]() 小于(或<) 白色沉淀 二 NaOH与稀盐酸反应生成的NaCl也能与AgNO3反应,得到白色沉淀,不能确定溶液中含有HCl(其他合理答案均给分)
小于(或<) 白色沉淀 二 NaOH与稀盐酸反应生成的NaCl也能与AgNO3反应,得到白色沉淀,不能确定溶液中含有HCl(其他合理答案均给分)
【解析】
烧杯②的外壁发烫,这是由于氢氧化钠固体溶于水时会放热,氢氧化钠溶液显碱性,使无色酚酞试液变红,故烧杯③的溶液呈红色。
氢氧化钠与稀盐酸反应生成氯化钠和水,反应的化学方程式为![]() 。
。
[实验探究]:
方案一:测定反应后溶液的pH值,若pH值小于7,则盐酸过量;
方案二:滴加AgNO3溶液,银离子与氯离子结合生成白色沉淀;
故有:
方案 | 方案一 | 方案二 | 方案三 |
实验操作 | 用洁净的玻璃棒蘸取反应后溶液,滴到pH试纸上,将试纸显示的颜色与标准比色卡比较 | 取适量反应后溶液于试管中,滴加AgNO3溶液 | 取适量反应后溶液于试管中,滴加Na2CO3溶液 |
实验现象 | 试纸变为红色,pH小于(或<)7 | 有白色沉淀生成 | 有气泡冒出 |
实验结论 | 稀盐酸过量 | 稀盐酸过量 | 稀盐酸过量 |
[交流讨论]:
上述三个方案中方案二不能达到探究目的,理由是NaOH与稀盐酸反应生成的NaCl也能与AgNO3反应,得到白色沉淀,不能确定溶液中含有HCl(其他合理答案均给分)。

 一线名师提优试卷系列答案
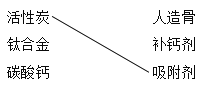
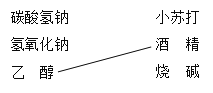
一线名师提优试卷系列答案【题目】(1)补齐连线。________
A组 物质——用途 | B组 物质——俗称 |
|
|
(2)金属在人类的生活、生产中被广泛应用。
①《国家宝藏》节目介绍了云南省博物馆馆藏青铜文物——四牛金骑士铜贮贝器。青铜是重要的铜合金,其硬度_______(填“大于”或“小于”)纯铜。铜常用作导线,利用了铜的_______和延展性。
②地球上的金属资源广泛地存在于地壳和海洋中,地壳中含量最多的金属元素是_______。人类每年要从矿石中提取大量的金属,提取量最大的是铁,磁铁矿的主要成分是_______。