题目内容
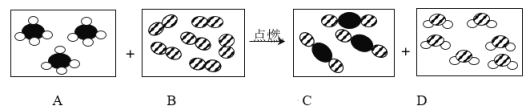
【题目】化学兴趣小组对“蜡烛及其燃烧”进行探究。
(查阅资料)蜡烛的主要成分是石蜡,石蜡由碳、氢两种元素组成。
问题一:蜡烛燃烧的产物是什么?
问题二:燃着的蜡烛在密闭容器中熄灭的原因是什么?
(作出猜想)问题一:蜡烛燃烧的产物含有二氧化碳和水;除了上述猜想,你的猜想:燃烧产物可能还含有_____。
问题二:熄灭的原因是燃烧消耗完了氧气;熄灭的原因是二氧化碳含量增多。
(实验1)(1)用冷而干的小烧杯罩在蜡烛火焰上,观察到_____,证明有水生成。
(2)用内壁涂有澄清石灰水的小烧杯罩在蜡烛火焰上,观察到_____证明有二氧化碳生成。二氧化碳和石灰水反应的化学方程式为_____。
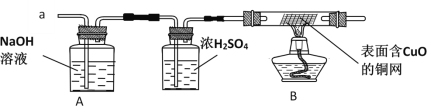
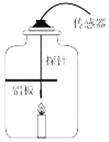
(实验2)在老师的帮助下,在如图所示装置中,点燃蜡烛至熄灭,利用多功能传感器测量了有关量。实验结束后,发现黑色固体颗粒附着在铝板表面,同时传感器获得的实验前后有关数据如表所示:
相对湿度 | 氧气含量 | 二氧化碳含量 | 一氧化碳含量 | |
蜡烛点燃前 | 36.4% | 21.2% | 0.058% | 0 |
蜡烛熄灭后 | 72.6% | 15.6% | 3.843% | 0.0192% |
(实验结论)由实验及结果,蜡烛燃烧生成的产物是_____;密闭容器内蜡烛熄灭的原因是_____。
(反思拓展)含碳燃料不充分燃烧会生成一氧化碳等物质,既浪费资源,又污染空气。为使燃料充分燃烧,应采取的措施是_____(答一条即可)。
【答案】一氧化碳 烧杯内壁出现水珠 澄清的石灰水变浑浊 Ca(OH)2+CO2═CaCO3↓+H2O 水、二氧化碳和一氧化碳 氧气的量不足 增大可燃物与氧气的接触面积
【解析】
[作出猜想]蜡烛的主要成分是石蜡,石蜡由碳、氢两种元素组成,所以蜡烛燃烧的产物含有二氧化碳和水,还可能生成一氧化碳;故填:一氧化碳;
[实验1](1)用干冷的小烧杯罩在蜡烛火焰上,观察到烧杯内壁出现水珠,证明有水生成。故填:烧杯内壁出现水珠;
(2)二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;故填:澄清的石灰水变浑浊;Ca(OH)2+CO2═CaCO3↓+H2O;
[实验2][实验结论]由实验及结果反应前氧气的体积分数是18.7%,当氧气的体积分数达到15.6%时,蜡烛熄灭,说明氧气的浓度低于一定值时,蜡烛无法燃烧,故密闭容器内蜡烛熄灭的原因是:氧气的量不足;由表中数据可知:反应前二氧化碳和一氧化碳的体积分数分别是0.058%、0%,反应后二氧化碳和一氧化碳的体积分数分别是3.643%、0.018%.反应前后湿度增加,那么蜡烛燃烧是有水生成的;说明蜡烛燃烧生成的产物是水、二氧化碳和一氧化碳。故填:水、二氧化碳和一氧化碳;氧气的量不足;
[反思拓展]为了充分燃烧可以增大可燃物与氧气的接触面积。故填:增大可燃物与氧气的接触面积。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案【题目】氧气是我们身边无法离开的物质。某兴趣小组对氧气的研究如下:
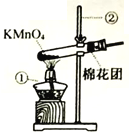
I.氧气的制备:
(1)写出上图中有标号仪器的名称:①___________,②__________。
(2)写出用KMnO4制取O2的化学反应方程式__________________。该装置中棉花团的作用是_________________,图中装置一处明显的错误是______________。
II.氧气的收集:
[实验1]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验3次。
[实验2]用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40秒,测定瓶中氧气的含量,重复实验3次。
[实验3]用排水法收集氧气,测定瓶中氧气的含量,重复实验3次。
实验数据:
实验1 | 实验2 | 实验3 | |||||||
氧气的体积分数(%) | 79.7 | 79.6 | 79.9 | 88.4 | 89.0 | 87.9 | 90.0 | 89.8 | 89.3 |
氧气的平均体积分数(%) | 79.7 | 88.4 | 89.7 | ||||||
数据
(3)由实验1、2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是_______________。
(4)不考虑操作因素,实验3获得的氧气体积分数不能达到100%的主要原因是_______。
Ⅲ.铁丝在氧气中燃烧
(5)铁丝在纯净氧气中燃烧的化学反应方程式为________________________。
(6)铁丝燃烧时火星四射,经研究表明产生火星四射现象的原因,可能是同时生成了某种气体,推测该气体是_____________(填化学式)。将燃烧后的黑色固体粉碎后,滴加稀盐酸,若产生气泡,则原因是________________(用化学反应方程式表示)。
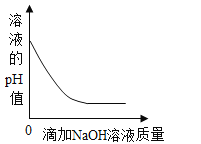
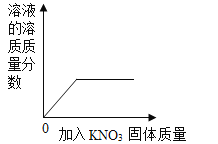
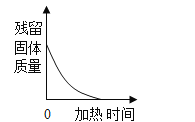
【题目】下列四个图象中,能正确反映对应变化关系的是( )
|
|
|
|
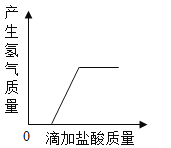
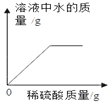
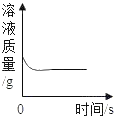
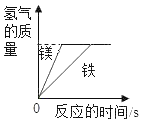
A.向一定质量的氢氧化钠溶液中加入稀硫酸至过量 | B.向一定质量的稀硫酸中加入锌片 | C.常温下,足量的镁、铁分别同时放入少量等质量、等质量分数的稀盐酸中 | D.向一定质量的二氧化锰中加入过氧化氢溶液 |
A. AB. BC. CD. D