题目内容
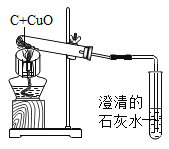
【题目】下图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器,欲利用其进行下列化学实验。
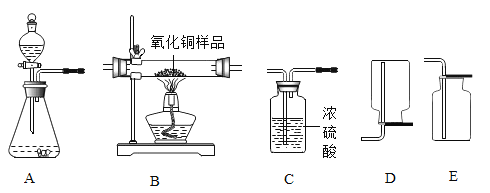
(1)以锌和稀硫酸为原料,制取并收集干燥的氢气
①所选仪器的连接顺序为_____(从左到右填写仪器序号字母)。
②生成氢气时,装置A中所发生反应的化学方程式为_____。
③装置A中使用分液漏斗的优点除节的药品外,还有_____(写一条即可)。
④反应结束后,装置A中溶液的pH与之前相比_____(填“增大”“减小”“不变”“无法判断”之一)。
⑤下列关于氢气的叙述不正确的是_____(选填下列序号之一)。
A 氢气作燃料的优点是燃烧热值高,产物无污染
B 保持氢气化学性质的最小微粒是氢原子
C 点燃氢气前,一定要检验氢气的纯度
D 氢气除用排空气法收集外,还可以用排水法收集
(2)若用锌和稀硫酸反应制取氢气,并用来测定某20g不纯氧化铜样品的纯度(杂质不反应),仪器连接顺序为:A→C1→B→C2→C3(已知![]() ;C1、C2、C3为三个盛浓硫酸的洗气瓶)。
;C1、C2、C3为三个盛浓硫酸的洗气瓶)。
①在该装置连接中,洗气瓶C1、C2的作用分别是_____。
②装置B中大玻璃管内的现象是_____。
③若经过充分反应,测得反应前、后洗气瓶C2的质量增加3.6g,则原氧化铜样品中氧化铜的纯度是_____。
【答案】ACD ![]() 控制化学反应速率 增大 B 除去氢气中的水蒸气,吸收氢气和氧化铜反应生成的水 黑色粉末变成红色 80%
控制化学反应速率 增大 B 除去氢气中的水蒸气,吸收氢气和氧化铜反应生成的水 黑色粉末变成红色 80%
【解析】
锌和稀硫酸反应生成硫酸锌和氢气,氢气和氧化铜加热生成铜和水。
(1)①锌和稀硫酸反应生成硫酸锌和氢气,反应在常温下进行,方法装置选用A,收集干燥的氢气,需要用浓硫酸吸收水分,氢气密度比空气小,用向下排空气法收集,收集装置选用D,故所选仪器的连接顺序为ACD。
②生成氢气时,装置A中所发生反应是锌和稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为![]() 。
。
③装置A中使用分液漏斗的优点除节的药品外,可以控制稀硫酸的滴加速率,进而控制化学反应速率,故还有控制化学反应速率。
④反应前,滴加稀硫酸,溶液显酸性,锌和稀硫酸反应生成硫酸锌和氢气,硫酸锌显中性,故反应结束后,装置A中溶液的pH与之前相比增大。
⑤A、氢气燃烧生成水,则氢气作燃料的优点是燃烧热值高,产物无污染,故A正确;
B、氢气由氢气分子构成,则保持氢气化学性质的最小微粒是氢分子,故B不正确;
C、氢气属于可燃性气体,不纯点燃会发生爆炸,则点燃氢气前,一定要检验氢气的纯度,故C正确;
D、氢气密度比空气小,不溶于水,则氢气除用排空气法收集外,还可以用排水法收集,故D正确。故选B。
(2)①A装置和C1相连,则C1的作用是除去氢气中的水蒸气,B装置和C2相连,氢气和氧化铜加热生成铜和水,则C2的作用是吸收氢气和氧化铜反应生成的水,故在该装置连接中,洗气瓶C1、C2的作用分别是除去氢气中的水蒸气,吸收氢气和氧化铜反应生成的水。
②氢气和氧化铜加热生成铜和水,故装置B中大玻璃管内的现象是黑色粉末变成红色。
③经过充分反应,测得反应前、后洗气瓶C2的质量增加3.6g,则氢气和氧化铜反应生成水的质量为3.6g
设氧化铜的质量为x
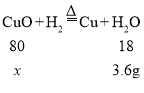
![]()
![]()
故原氧化铜样品中氧化铜的纯度是![]() 。
。

 阅读快车系列答案
阅读快车系列答案