题目内容
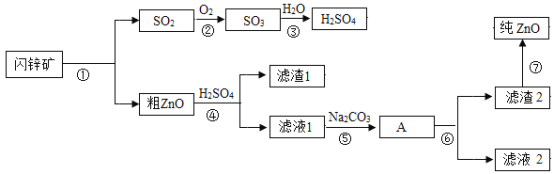
【题目】某工业废液中含有KCl和CaCl2,如果将该废液中的KCl和CaCl2分离回收变废为宝,设计工艺流程如下图所示,回答问题。

(1)操作2的名称是_____。
(2)写出固体B的化学式_____。
(3)向固体A中加适量稀盐酸的作用是_____。
【答案】蒸发 KCl 将CaCO3沉淀转化为CaCl2
【解析】
工业废液中含有KCl和CaCl2,先加入试剂A,会产生溶液和固体,则试剂A为碳酸钾,碳酸钾和氯化钙反应生成碳酸钙沉淀和氯化钾,过滤之后,得到溶液a是氯化钾和碳酸钾溶液,固体A是碳酸钙,再向溶液a中加入适量稀盐酸,稀盐酸和碳酸钾反应生成氯化钾、二氧化碳和水,得到氯化钾溶液,再经过蒸发结晶最终得到氯化钾晶体;向碳酸钙固体中加入适量盐酸,碳酸钙和盐酸反应生成氯化钙、二氧化碳和水,得到氯化钙溶液,再经过蒸发结晶最终得到氯化钙晶体;
(1)根据分析可知,操作2的名称是蒸发;
(2)根据分析可知,固体B是氯化钾,化学式为KCl;
(3)根据分析可知,向固体A中加适量稀盐酸的作用是将CaCO3沉淀转化为CaCl2。

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目