题目内容
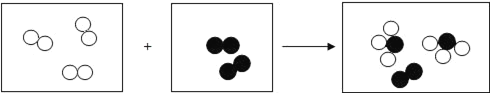
【题目】银器发暗是因为形成了黑色的Ag2S。欲使银器变亮,可先用洗衣粉洗去表面油污,再把它和铝片放入碳酸钠溶液中共煮,至银器恢复银白色时,取出银器,用水洗净即可。发生反应的化学方程式为:2Al+3Ag2S+6H2O![]() 6Ag+2Al(OH)3+3X↑,X的化学式是
6Ag+2Al(OH)3+3X↑,X的化学式是
A. H2SB. SO2C. SO3D. O2
【答案】A
【解析】
由2A1+3Ag2S+6H2O![]() 6Ag+2Al(OH)3+3X↑可知,反应前后铝原子都是2个,银原子都是6个,根据质量守恒定律,在化学反应中原子的种类和数目不变,反应前的硫原子是3个,反应后应该是3个,包含在3X中,反应前氢原子是12个,反应后应该是12个,其中6个包含在3X中,反应前、后的氧原子都是6个,因此X化学式是H2S。故选A。
6Ag+2Al(OH)3+3X↑可知,反应前后铝原子都是2个,银原子都是6个,根据质量守恒定律,在化学反应中原子的种类和数目不变,反应前的硫原子是3个,反应后应该是3个,包含在3X中,反应前氢原子是12个,反应后应该是12个,其中6个包含在3X中,反应前、后的氧原子都是6个,因此X化学式是H2S。故选A。

 53随堂测系列答案
53随堂测系列答案【题目】日常生活中,每位同学都会接触到硬水。咸宁市某校化学兴趣小组的同学在老师的带领下对硬水进行了一些探究和拓展实验。
(查阅资料)水的硬度是由水中溶解的可溶性钙和镁化合物引起的,硬水中溶解的钙和镁化合物可分为两类:钙、镁的碳酸氢盐;钙、镁的硫酸盐或氯化物,一般所说的水的硬度是由上述两类化合物引起的。
(1)日常生活中常用煮沸的方法将硬水软化,这种方法可靠吗?小组同学设计了如下模拟实验。
实验序号 | 实验操作 | 实验现象 |
Ⅰ | 分别取适量碳酸氢钙溶液和氯化钙溶液于A、B两支试管中,同时加热 | A试管中产生气泡,有沉淀生成,B试管中无明显现象。 |
Ⅱ | 冷却后,在上述实验后两支试管中,分别滴加几滴肥皂水,振荡 | ①_____(填“A”或“B”)试管中有较多泡沫,另一支试管中泡沫较少。 |
实验结果:用煮沸的方法可以降低水的硬度。
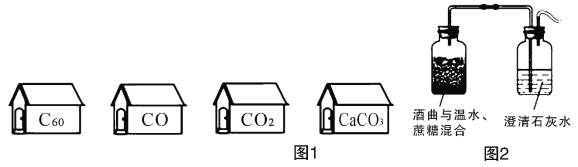
(2)小组同学对硬水中为什么含有碳酸氢钙非常感兴趣,于是再次学习九年级化学下册课本中的资料卡片:石笋和钟乳石的形成。知道了当石灰岩遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:CaCO3+CO2+H2O═Ca(HCO3)2
小组同学思考:若向碳酸钠溶液中通入一定量的二氧化碳,是否也能生成碳酸氢钠?
于是他们对此开始实验探究(不考虑二氧化碳和碳酸作为溶质的情况)
(提出问题)所得溶液中溶质是什么?
(提出猜想)
猜想一:溶质为Na2CO3;猜想二:溶质为 NaHCO3;猜想三:溶质为②_____。
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
a.取所得溶液少许于试管中,向其中滴加过量的CaCl2溶液 | 有白色沉淀生成 | 猜想二③_____ (填“成立”或“不成立”) |
b.取实验步骤a中上层清液,滴加适量稀盐酸 | 有气泡冒出 | 猜想一不成立 |
写出实验步骤b中发生反应的化学方程式④_____。
通过实验,小组同学得出了正确结论。
(3)热水瓶用久后,瓶胆内壁常附着一层水垢,老师说其成分主要是碳酸钙、氢氧化镁等。小组同学认为可使用稀盐酸除去,请写出发生中和反应的化学方程式⑤_____。
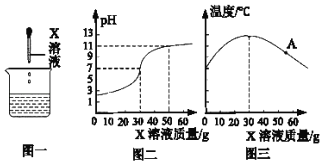
(4)小组同学还对稀盐酸和氢氧化钠溶液发生中和反应进行了如下探究:
用pH传感器测得烧杯内溶液的pH变化图象(如图二),同时用温度传感器测得烧杯内温度变化图象(如图三),实验过程中保温良好,忽略热量散失。
Ⅰ.请分析图三,能得到什么结论⑥_____。
Ⅱ.图三中A点对应溶液的溶质成分是⑦_____ (填写化学式)。