题目内容
硫酸和氢氧化钠是我们学过的两种重要的物质,请按要求填空.
(1)将无色酚酞溶液滴入氢氧化钠溶液中,溶液变为 色.
(2)将NaOH固体长期放置在空气中,氢氧化钠会与空气中的 发生反应而变质.
(3)实验室常用浓硫酸作干燥剂,说明浓硫酸具有 性.
(4)写出稀硫酸与氢氧化钠溶液反应的化学方程式: .
(1)将无色酚酞溶液滴入氢氧化钠溶液中,溶液变为
(2)将NaOH固体长期放置在空气中,氢氧化钠会与空气中的
(3)实验室常用浓硫酸作干燥剂,说明浓硫酸具有
(4)写出稀硫酸与氢氧化钠溶液反应的化学方程式:
考点:碱的化学性质,浓硫酸的性质及浓硫酸的稀释,中和反应及其应用,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性,常见的碱 碱的通性
分析:(1)从酚酞溶液是酸碱指示剂,遇酸不变色,遇碱变红色去分析;
(2)从氢氧化钠会与空气中的C02反应生成碳酸钠而变质去分析;
(3)从浓硫酸具有吸水性去分析;
(4)从稀硫酸与氢氧化钠溶液反应生成硫酸钠和水去分析.
(2)从氢氧化钠会与空气中的C02反应生成碳酸钠而变质去分析;
(3)从浓硫酸具有吸水性去分析;
(4)从稀硫酸与氢氧化钠溶液反应生成硫酸钠和水去分析.
解答:解:(1)酚酞溶液是酸碱指示剂,遇酸不变色,遇碱变红色,所以将无色酚酞溶液滴入氢氧化钠(碱)溶液中,溶液变为红;故答案为:红;
(2)将NaOH固体长期放置在空气中,氢氧化钠会与空气中的C02反应生成碳酸钠而变质;故答案为:二氧化碳;
(3)由于浓硫酸具有吸水性,所以实验室常用浓硫酸作干燥剂;故答案为:吸水;
(4)稀硫酸与氢氧化钠溶液反应生成硫酸钠和水,其化学方程式为:H2SO4+2NaOH═Na2SO4+2H2O;故答案为:H2SO4+2NaOH═Na2SO4+2H2O.
(2)将NaOH固体长期放置在空气中,氢氧化钠会与空气中的C02反应生成碳酸钠而变质;故答案为:二氧化碳;
(3)由于浓硫酸具有吸水性,所以实验室常用浓硫酸作干燥剂;故答案为:吸水;
(4)稀硫酸与氢氧化钠溶液反应生成硫酸钠和水,其化学方程式为:H2SO4+2NaOH═Na2SO4+2H2O;故答案为:H2SO4+2NaOH═Na2SO4+2H2O.
点评:本题综合性较强,考查学生对氢氧化钠的化学性质及相关化学方程式的书写,是考试的重点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
小明发现父亲正欲将草木灰(呈碱性)与一种化肥混合,小明向父亲提示:此化肥不易与草木灰混合,否则会使其中的肥效受到损失.你认为是下列化肥中的( )
| A、KNO3 |
| B、CO(NH2)2(尿素) |
| C、NaNO3 |
| D、NH4HCO3 |
在AgNO3、Mg(NO3)2和Cu(NO3)2的混合溶液中,加入一定量的铁粉充分反应后,过滤,洗涤,将滤渣放入盐酸中有气泡产生,滤液中存在的阳离子是( )
| A、Cu2+ |
| B、只有Fe3+ |
| C、Fe2+ |
| D、Mg2+、Fe2+ |
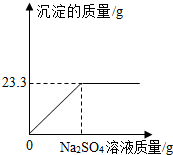 称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4+↓+2NaCl)
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4+↓+2NaCl) 针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠反应可产生SO2气体:设计实验如图所示.
针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠反应可产生SO2气体:设计实验如图所示. “侯氏制碱法”制得的纯碱中通常含有少量的氯化钠.某同学想测定含有少量氯化钠杂质的纯碱样品中碳酸钠(Na2CO3)的质量分数.该同学操作如下:现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试问答问题:
“侯氏制碱法”制得的纯碱中通常含有少量的氯化钠.某同学想测定含有少量氯化钠杂质的纯碱样品中碳酸钠(Na2CO3)的质量分数.该同学操作如下:现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试问答问题: